Inscription / Connexion Nouveau Sujet
titrage
Bonjour,
Je dois réaliser cet exercice mais je ne sais pas de tout comment commencer .
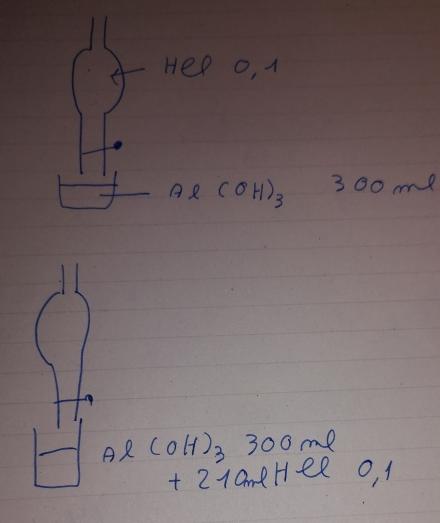
On titre 300 ml de Al(OH)3 par HCl 0,1 M . Le point d'équivalence apparaît après ajout de 210 ml de HCl .
Calculer la concentration de Al(OH)3
Ce que j'ai essaie de faire
Je me suis dis que
V1 = 300 ml
C1= 0.1
V2= 300+210= 510 ml
C2?
c2= ( 0,1 x 300) / 510 = 0,05
Voilà je sais que j'ai completement faux, est ce que vous pouvez m'aider svp merci beaucoup
Bonsoir,
Pourrais-tu commencer par mettre à jour ton profil pour nous dire quel est ton niveau d'étude :
 extrait de
extrait de Q12 - Dois-je forcément indiquer mon niveau lorsque je poste un nouveau topic ?
Pour un exercice de dosage, la première des choses est de faire un schéma simplifié sur dispositif avec les données principales fournies par l'énoncé (tu es sûr(e) de l'avoir recopié au mot près ?) :
 extrait de
extrait de Q05 - Puis-je insérer une image dans mon message ? Comment faire ? Quelle image est autorisée ?
Ensuite, il faut écrire l'équation-bilan de la réaction en présence.
Puis établir la condition d'équivalence rappelée dans cette fiche (clique sur la maison) :

Merci de ta réponse,
oui j'ai recopier mots pour mots l'énoncé
est ce que l'équation c'est
Al(OH)3 + HCl -> AlCl3 +H2O
oui j'vais déjà regarder cette fiche 
est ce que la solution est
C= (0,1 x 210)/ 300 = 0,07
Ton équation n'est pas correcte car elle ne représente par la réaction en jeu.
Par exemple la solution d'hydroxyde d'aluminium est (Al3+ + 3OH-) et non Al(OH)3 qui est le composé ionique avant sa dissolution dans l'eau.
Idem pour HCl
Ensuite, un résultat non justifié et sans calcul littéral avant de finir une application numérique n'a aucun sens. De même s'il est sans unité.

est ce que maintenant mon equation est correct
Al(OH)3 + HCl -> Al3+ + 3OH- + Cl- + H+
C Al(OH)[sub]3[/sub] = ( C HCl x VHCl) / VAl(OH)[sub]3[/sub]
= (0,1 x 210) / 300 = 0.07
Al(OH)3 + HCl -> Al3+ + 3OH- + Cl- + H+
C Al(OH)[sub]3[/sub] = ( C HCl x VHCl) / VAl(OH)[sub]3[/sub]
= (0,1 x 210) / 300 = 0.07
est ce que maintenant mon equation est correct
Al(OH)3 + HCl -> Al3+ + 3OH- + Cl- + H+
C Al(OH)3 = ( C HCl x VHCl) / VAl(OH)3
= (0,1 x 210) / 300 = 0.07
Le mieux serait de déduire les formules des deux solutions aqueuses.
Ensuite, fait un schéma du dispositif avec toutes les données de l'énoncé (le schéma de la fiche peut servir d'inspiration)
Enfin, écris l'équation-bilan avec uniquement les réactifs en jeu (et pas les ions spectateurs).


 équivalences des systèmes de niveaux scolaires
équivalences des systèmes de niveaux scolaires