Inscription / Connexion Nouveau Sujet
Photon absorption
Bonjour j'ai besoin de votre aide pour l'exercice suivante :
1) Prévoir à l'aide du doc 2, si avec un atome d'hydrogène dans l'état d'énergie n=3, on peut absorber un photon dont l'énergie vaut E= 0,97 eV, puis un photon dont l'énergie vaut E = 1,20 eV . Justifier votre réponse.
2)Prévoir à l'aide du doc 3, si du silicium solide peut absorber un photon dont l'énergie vaut E = 0,97 eV, puis un photon dont l'énergie vaut E= 1,20 eV. Justifier votre réponse.
Mes réponses:
1) Pour le photon dont l'énergie vaut E=0,97 eV:
Ici on a -1,51+0,97 = -0,54 eV . Ce résultat négatif montre que l'absorption est possible.
Pour le photon dont l'énergie vaut E=1,20 eV :
Ici on a -1,51+1,20= -0,31 eV. Ce résultat négatif montre aussi que l'absorption est possible
2)Pour le photon dont l'énergie vaut E=0,97 eV:
On sait que Eg = 1,12 donc Eg>E, l'absorption n'est pas possible.
Pour le photon dont l'énergie vaut E=1,20 eV on a Eg<E, l'absorption est possible.
Merci si vous me confirmez, bonne soirée
** image supprimée **
Bonjour,
Attention, seuls les schémas accompagnant l'énoncé peuvent être joints (spectre absorptions, diagramme des niveaux d'énergies quantifiés, ...) mais le texte doit être entièrement recopié :
 extrait de
extrait de Q05 - Puis-je insérer une image dans mon message ? Comment faire ? Quelle image est autorisée ?

Bonjour, désolé pour cette infraction, je vous remets ci-joint les informations importantes des doc 2 et 3 :
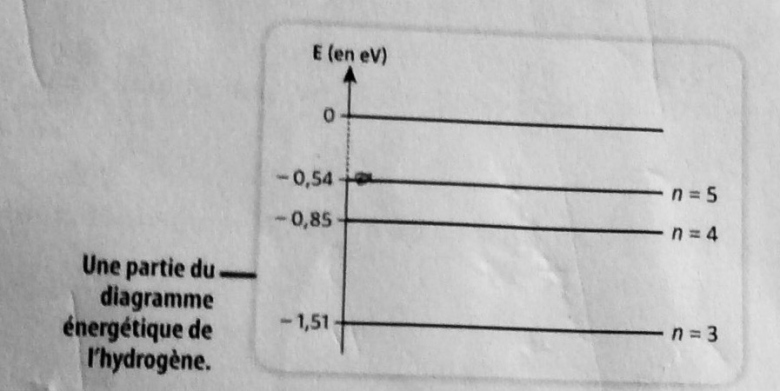
Voici les informations importantes du doc 2 (accompagnées par une partie du diagramme énergétique de l'hydrogène en image): « La valeur de l'énergie d'un photon émis est égale à la différence d'énergie (en valeur absolue) qui existe entre deux niveaux possibles, c'est-à-dire entre deux états d'énergie possibles de l'atome. Ce sont donc uniquement les photons identiques à ceux émis qui pourront être absorbés par cet atome. L'analyse de la lumière absorbée permet ainsi d'identifier cet atome. »
Voici ici les informations importantes du doc 3: « Dans les solides, qui peuvent être considérés comme des assemblages d'atomes, ce ne sont plus des niveaux d'énergie mais des bandes d'énergie qui sont permises et qui sont séparées par des bandes interdites. Au repos, des électrons se trouvent dans la bande de valence. L'énergie Eg (ou gap) à apporter à un électron pour qu'il franchisse la bande interdite d'un semi-conducteur peut être fournie par un photon, d'énergie égale ou supérieure à Eg. Pour le silicium par exemple, Eg= 1,12 électron-volt. »
Merci si vous m'aidez, bonne journée
Bonjour. Pour le 1) j'ai un gros doute, ce n'est pas le contraire plutôt ? (Il faut que le résultat soit positif pour montrer que l'absorption soit possible...)
Merci pour votre aide, bonne journée
Bonjour, désolé pour la réponse tardive,
Pour ta première question, je te rappelle ton cours là-dessus (clique sur la maison) : ![]() Modèle ondulatoire et particulaire de la lumière
Modèle ondulatoire et particulaire de la lumière
En effet, l'énergie d'un atome est quantifiée, elle ne peut donc prendre que certaines valeurs bien déterminées. On dit que l'atome ne peut exister que dans dans un nombre discret de niveaux d'énergie.
Ici on te fournit les niveaux d'énergie, tu vois bien qu'avec un photon d'énergie 0,97 eV on passe bien de l'état d'énergie n = 3 à n = 5.
Ce qui n'est pas possible pour l'autre photon d'énergie 1,20 eV, puisque cela n'aboutirait à aucun état d'énergie de l'atome d'hydrogène.

Bonsoir, désolé également pour ma réponse tardive .
Votre explication est très claire, merci pour votre aide.
Bonne soirée .


