Inscription / Connexion Nouveau Sujet
Le protoxyde dazote
Bonsoir, quelqu'un pourrait m'aider à répondre au question 2.b, 6.c et 7.
Le protoxyde d'azote N20 (g) est un gaz utilisé pour améliorer les performances des moteurs de voitures par un apport de dioxygène. Rendus populaires dans le film Fast and Furious, les systèmes NOS (Nitrous Oxide Systems) permettent d'injecter le protoxyde d'azote N,0(g) dans la chambre de combustion du moteur, en même temps que l'air et l'essence. Lors de la compression, le gaz se réchauffe, se décompose en produisant du dioxygène selon la réaction d'équation N20 (g) → N2 (g) +1/2 O2 (g).
Pour étudier la cinétique de cette décomposition, on introduit, dans un récipient de volume V constant, une quantité no = 41,3 mmol de protoxyde d'azote et on relève, au cours du temps, la pression P des gaz dans l'enceinte. La température T est maintenue à 600 °C. Les résultats sont rassemblés dans le tableau ci-dessous :
t (min): 0 12 25 45 90
P (bar)1,000 1,062 1,120 1,195 1,314
1. Citer un capteur ayant permis de suivre l'évolution du système.
Capteur de pression
2. a. La réaction étudiée est-elle lente ou rapide ? Rapide
b. Dans le moteur, la combustion entraîne une forte élévation de la température qui peut atteindre 2 000 °C. Justifier l'utilisation du protoxyde d'azote pour obtenir rapidement un gain de puissance.
3. Établir un tableau d'avancement du système.
4. a. Exprimer la pression initiale P, en fonction de no, R, Tet V où R est la constante du gaz parfait.
Exprimer n(N2O) en fonction de no, P et Po.
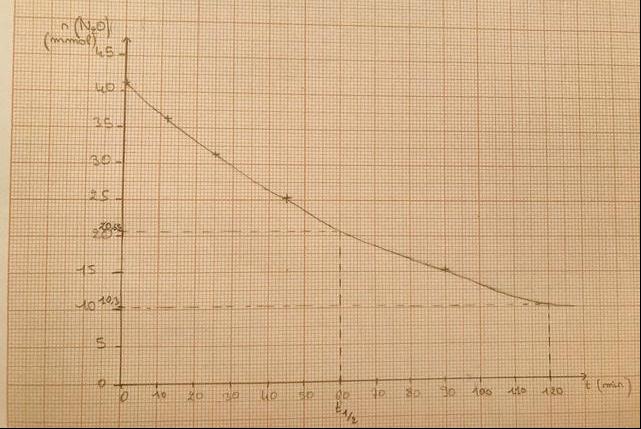
5. a.Tracer l'évolution de la quantité n(N2O) au cours du temps.
b.Déterminer la quantité n(N,O), à t1 =2x t1/2.
c. Comparer n(N20)t1 et no/2. Pourquoi peut-on conclure que la réaction est d'ordre 1 par rapport à N20 ?
7. Quelle est l'influence d'une admission plus importante de protoxyde d'azote sur la vitesse du véhicule ?
Merci
Bonjour,
Bienvenue sur le forum !
En vertu de ceci :
Pourrais-tu nous dire ce que tu as été en mesure de faire et éventuellement proposer tes pistes de réflexion sur celles qui te posent problème ?

Bonsoir, Voici ce que j'ai fait:
1. Capteur de pression
2. a.Réaction rapide
b. J'ai deux propositions de réponse : puisque la température est un facteur cinétique la combustion permet d'augmenter la température et donc d'accélérer la réaction de combustion de l'essence ou bien l'augmentation de la température lors des combustions provoque un besoin en O2 plus important et donc il faut plus du N2O pour produire du O2.
3. Tableau d'avancement :
N2O > N2 + O2
no 0 0
no-x. x. 1/2x
no-xmax. xmax. 1/3x max
4.a Po=noRT/v
b. n(N2O) = no -2 *no*(P/Po-1)
= no(3-2P/Po)
6.a. Après avoir tracé le graphique, on lit t1/2=60 min (no/2=20,65mmol)
b. t1=2*60= 120 min
Graphiquement, n(N20) = 10,3 mmol.
( je n'ai pas réussi à poste le graphique ).
Je n'ai pas trouvé pour les 2 dernière question.
1. OK
2. a. Pourquoi ? Pourrais-tu tracer la courbe pour dire ça ?
 extrait de
extrait de Q05 - Puis-je insérer une image dans mon message ? Comment faire ? Quelle image est autorisée ?
b. Il suffit de lire l'énoncé :
Lors de la compression, le gaz se réchauffe, se décompose en produisant du dioxygène selon la réaction d'équation N20 (g) → N2 (g) +1/2 O2 (g).
Quelle proposition est donc vraie ?
3. A reprendre, il y a 2 fautes d'inattention dans ce que tu proposes.
4. a. Tu n'expliques pas ce que tu fais, c'est incompréhensible en l'état
6. Tu n'as pas recopié la question et ça serait bien d'avoir la courbe en question.

2.a Étant donné que la combustion de l'essence doit être rapide et on continue celle du N2O doit également être rapide.
2.b J'imagine que c'est de la deuxième proposition : l'augmentation de la température provoque un besoin de O2 apporté par la combustion du N2O
3. Le coefficient est toujours 1/2.
Je n'arrive pas à poster le graphique car le fichier est trop volumineux. Comment je peux faire ?
Tu peux les enregistrer au format .gif pour réduire leur taille si tu travailles avec le PC. Ou alors aller dans les paramètres de ton téléphone et réduire la résolution de tes photos.

Merci, je vais te fournir ce lien car l'exercice avait déjà été traité : ![]() Cinétique chimique
Cinétique chimique
A disposition en cas d'interrogation 
Bonjour, j'ai déjà vu cet exercice mais les dernières questions que j'ai pas compris ne sont pas traités.
Il resterait donc celles-ci ?
c. Comparer n(N20)t1 et no/2. Pourquoi peut-on conclure que la réaction est d'ordre 1 par rapport à N20 ?
7. Quelle est l'influence d'une admission plus importante de protoxyde d'azote sur la vitesse du véhicule ?
Merci
Quelle est la définition d'une réaction d'ordre 1 ?
Je sais que pour une réaction d'ordre 1 la concentration du réactif est proportionnelle à la vitesse volumique. De plus graphiquement, la représentation graphique d'une réaction d'ordre 1 est une fonction exponentielle décroissante. Est-ce que ça te répond est correct : puisque la représentation graphique que j'ai obtenu correspond à celle d'une fonction exponentielle décroissante alors il s'agit d'une réaction d'ordre 1.
n(N2O)t1 est la moitié de no/2. Mais je ne sais pas comment utiliser cette information pour prouver que c'est une réaction d'ordre 1.
à t = t1/2, n(t) = no(NO2)/2
à t' = 2t1/2, n(t') = n(t)/2 = no(NO2)/4
A l'image d'une loi de décroissance radioactive (si tu as fait le cours), on a effectivement affaire à une décroissance exponentielle caractéristique d'une réaction d'ordre 1.
On aurait pu aller plus loin en traçant la courbe
ln( n(NO2)/no(NO2)) = f(t) et constater que c'est une droite ...

D'accord merci.
Pour la question 7, j'ai une proposition de réponse mais c'est presque la même réponse que la question 2.b ce qui n'est normal : La combustion du protoxyde d'azote produit du O2 nécessaire à la combustion de l'essence. La combustion de l'essence et donc la vitesse du véhicule sera plus rapide.
Effectivement, si on a un combustion de l'essence plus conséquente, alors la puissance thermique générée par la combustion va générer une puissance mécanique plus conséquente (par le biais du vilebrequin) qui va être convertie en énergie cinétique pas le système de transmission. Le véhicule ira donc plus vite

Le gaz a besoin de se réchauffer pour se décomposer. Or dans une chambre à combustion la température est élevée ...

La combustion du N2O permet d'augmenter la température et donc d'accélérer la réaction de combustion de l'essence. C'est ça ?
N2O se décompose en N2 et O2 à haute température. Donc cette décomposition introduit davantage de O2 nécessaire à la combustion (qui se fait à haute température)


 moteur de recherche
moteur de recherche page de choix du forum
page de choix du forum fiches du site
fiches du site