Inscription / Connexion Nouveau Sujet
TP dosage par étalonnage
Bonjour,
je fais se poste car mon prof de physique m'a donné un TP a finir a la maison mais il y a des questions ou je ne suis pas du tout sur de moi
voici l'énoncé :
La dose journalière admissible (DJA) du bleu patenté est de 2,5 mg par kilogramme de masse corporelle. Un élève, pesant 60 kg, boit 0,2 L du sirop de menthe étudié.
On donne le matériel suivant : Colorimètre (qui fera office d'appareil de mesure de l'absorbance) et ses cuves, burettes graduées, tubes à essais avec support, pissette d'eau pure. Sirop de menthe dilué 10 fois. Eau distillée. Solution de bleu patenté de concentration C0=1,0.10^-5 mol/L".
question :
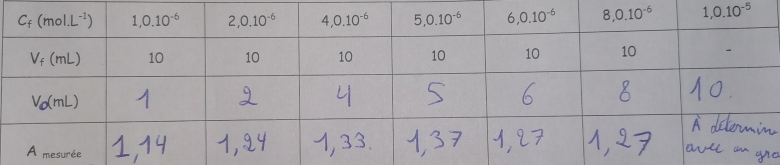
1) Proposer un protocole pour établir la courbe détalonnage absorbance A en fonction de la concentration C.
Sur un graphique on place sur la droite des ordonnées la quantité d'absorbance A des solutions connues par rapport à la concentration C des solutions connues ensuite on trace une droite qui passe par l'origine et les points des solutions connues . On obtient alors une courbe appelée courbe d'étalonnage.
2) quelle longueur d'onde doit-on travailler ?
650nm
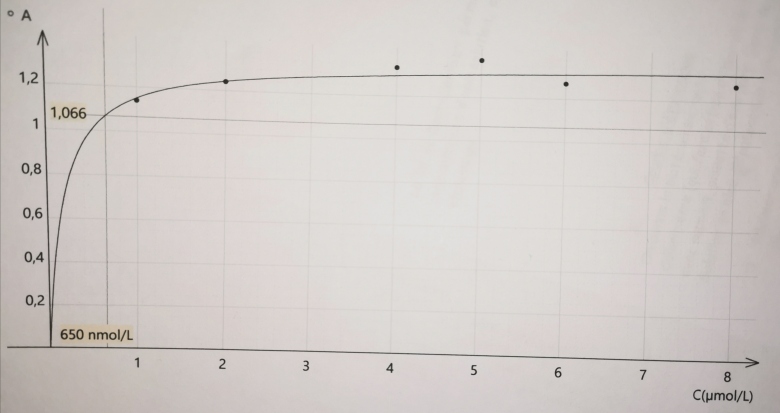
3) Tracer la courbe d'étalonnage A=f(C)
fichier ci-dessous
4) La loi de Beer-Lambert est elle vérifiée ? Justifier
je n'ai pas très bien compris ce qu'il veut qu'on fasse.
5) Expliquer la méthode pour déterminer la concentration en bleu patenté E131 dans le sirop de menthe
Grace à la loi de Beer-Lambert on peut déterminer la concentration d'une solution en réalisant un dosage par étalonnage. On doit simplement mesurer l'absorption connue et on obtient un point sur la courbe qui permet de déterminer la concentration en bleu patenté E131 dans le sirop de menthe.
6) L'élève a-t-il absorbé trop de colorant E131. On donne : M(E131)=1159,4 g/mol; densité du sirop de menthe 1,0.
Ici il faut utilisé une formule avec p mais on ne l'a jamais étudié en classe du coup je suis perdu.
merci d'avance pour votre aide!
Bonsoir,
Es-tu sûr d'avoir recopié fidèlement l'énoncé de ton TP ?
Il y a des choses qui m'interpellent, notamment la courbe d'étalonnage proposée qui n'est pas une droite passant par l'origine.
Tu devrais obtenir une droite comme proposée dans cette fiche : ![]() [lien]
[lien]

Merci pour votre réponse effectivement moi aussi cela m'a interpellé mais je vous assure que c'est les données relevés lors du TP
Est-ce que tu pourrais me fournir l'énoncé sous format pdf (un lien d'un hébergeur pdf par exemple) ?
Je suis preneur de ses commentaires également, histoire de comprendre ce qui nous a échappé  .
.
Je t'en prie, bonne journée
Bonjour,
Après avoir demandé à mon prof il m'a dit "ce n'est pas grave" et de faire avec les valeurs que j'ai obtenu même si les données ne sont pas proportionnelles.
Plus que bizarre ...
Autant dire que pour la question :
4) La loi de Beer-Lambert est elle vérifiée ? Justifier
Pour le coup, tu n'as pas de droite passant par l'origine la conclusion est donc vite vue.
Pour la 5, tu peux extrapoler avec la méthode vue en cours (ou dans la fiche fournie) mais ça n'a pas vraiment de sens de poursuivre, je suis assez surpris par la réponse de ton prof ...

Le pire c'est que quand je lui ai dit que ce n'était pas logique il m'a crié dessu et m'a dit que je suis censé le faire tout seul et qu'il ne devait pas m'aider du coup il ne m'a rien expliqué, mais pour la dernière question j'ai pas compris qu'elle formule il fallait utilisé pour répondre.
OK, longue vie à la pédagogie ...
Si tu as lu les deux liens fournis, maintenant que tu as tracé la courbe d'étalonnage, tu es censé, à partir de l'absorbance de la solution, en déduire la concentration de la solution cherchée.
Mais là, on pourrais faire une régression pour déterminer l'équation de la courbe mais ça n'a aucun sens 
Bonjour,
Le prof nous a envoyé un msg sur pronote mais vraiment je ne sais pas comment faire pour l1 question 6. Pouvez vous s'il vous plaît me dire qu'elle formule utilisé. Merci beaucoup pour votre aide !
Msg du prof :
TP dosage spectrophotométrique à rendre. Si la droite ne passe pas par zéro, ce n'est pas grave. Vous pouvez quand même appliquer la loi de Beer Lambert avec la solution de menthe de concentration en colorant E131 à déterminer
Bonjour,
On n'obtient pas une droite d'étalonnage vérifiant la loi de Beer-Lambert A = k x C mais ce n'est pas grave  ...
...
Pour répondre à ta question, l'énoncé te donne ceci :
La dose journalière admissible (DJA) du bleu patenté est de 2,5 mg par kilogramme de masse corporelle. Un élève, pesant 60 kg, boit 0,2 L du sirop de menthe étudié.
Donc V = 0,2 L.
A partir de la courbe étalonnage tu as pu déterminer la concentration en quantité de matière (ou molaire) du sirop de menthe.
Par définition de la concentration en quantité de matière :
et par définition de la quantité de matière
sachant que
On donne : M(E131)=1159,4 g/mol
Finalement, on peut écrire
Puis, ayant déterminé la masse en bleu de patenté absorbée, tu peux voir si la DJA est dépassée ou non.

OK merci, donc
J'ai relevé dans la courbe 650nmol/L en mol ça fait 6,5×10^-7
C= 6,5×10^-7
m = C×M×V
N.A
m= (6,5×10^-7)×(1159,4)×(0,2)
m= 0,000150722g en mg ça fait 0,150722 mg
On multiplie par 10 car la solution a été diluer 10 fois
Ça fait 1,50722
Dans l'énoncé on nous dit que l'élève pèse 60kg et le DJA c'est 2, 5mg par kg
Donc 2,5×60=150mg dose journalière
Donc l'élève n'a pas dépassé la dose journalière recommandée.
Bonsoir,
Mes commentaires :
OK merci, donc
J'ai relevé dans la courbe 650nmol/L en mol ça fait 6,5×10^-7 unité ?
Pourquoi donc ? Parce que l'absorbance mesurée pour le sirop dilué est A = ?
C= 6,5×10^-7 un résultat sans unité n'a aucun sens chimique
m = C×M×V définir les notations employées tel que proposé sur ta copie
N.A
m= (6,5×10^-7)×(1159,4)×(0,2)
m= 0,000150722g en mg ça fait 0,150722 mg trop de chiffres significatifs !
On multiplie par 10 car la solution a été diluer 10 fois non ! Un protocole de dilution se fait en raisonnant sur une conservation de la quantité de matière, lis cette fiche (clique sur la maison) :
Ça fait 1,50722 à reprendre, avec une unité cette fois
Dans l'énoncé on nous dit que l'élève pèse 60kg et le DJA c'est 2, 5mg par kg à reprendre
Donc 2,5×60=150mg dose journalière
Donc l'élève n'a pas dépassé la dose journalière recommandée.

OK donc c'est le grand C qu'on doit multiplier par 10 car c'est la concentration qui a été diviser par 10 au début ?
Ici on te précise que la solution mère a été diluée 10 fois, donc Cfille = Cmère/10 <=> Cmère = 10Cfille
Attention aux notations utilisées, il ne faut pas les changer en cours de route comme je viens de le faire.
Bonjour,
Désolé pour le délai de réponse, je suis rentré chez moi  .
.
Mais du coup la je multiplie la concentration que j'ai relevé grâce à la droite donc 6,5×10^-7×10
Encore une fois, un résultat sans unité n'a aucun sens chimique.
Mais oui : de l'absorbance mesurée, tu en déduis la concentration de la solution diluée 10 fois, puis tu en déduis la concentration de la solution mère

OK, donc
J'ai relevé dans la courbe 650nmol/L en mol ça fait 6,5×10^-7mol/L
C= 6,5×10^-7mol/L
m(E131) =C(E131) ×M(E131) ×V
N.A
C = (6,5×10^-7)×10 car la solution a été diluer 10 fois
m= (0.0000065)×(1159,4)×(0,2)
m= 0.00150722g en mg ça fait 1,50722mg
Dans l'énoncé on nous dit que l'élève pèse 60kg et le DJA c'est 2, 5mg par kg
Donc 2,5×60=150mg dose journalière
1,50722<150
Donc l'élève n'a pas dépassé la dose journalière recommandée.
Le raisonnement est correct mais attention au nombre de chiffres significatifs fournis : ![]() Les chiffres significatifs
Les chiffres significatifs

Oui effectivement j'avais remarqué après l'avoir posté je ferais attention la prochaine fois. Merci beaucoup pour votre aide très précieuse, ça m'a beaucoup aidé ! 



