Inscription / Connexion Nouveau Sujet
Titrage ions chlorure dans eau
Bonjour dans un TP de titrage des ions chlorure dans une eau de vichy il m es demandé
Les solutions ont été préparées avec l'eau distillé, aurait on pu utiliser de l'eau du robinet? Expliquer
Merci d'avance
Bonjour.
L'eau du robinet contient des espèces dissoutes qui, ajoutées à celles de l'eau de Vichy, risqueraient de fausser les résultats du titrage.
On évite ce problème en utilisant l'eau distillée qui est (en principe) pure.
Au revoir.
Bonjour J'ai un exercice dans mon tp de titrage des ions chlorure dans l'eau de vichy pour aller plus loin
Une eau industrielle contient des ions chlorure Cl- dont la concentration est égale à : [Cl-] = 8.0× 10 ^-3 mol/L. On souhaite mettre en évidence ces ions dans l'eau à l'aide d'une solution de nitrate d'argent dont la concentration en ions argent est noté [Ag+].
La solubilité du chlorure d'argent est s= 1.26×10^-5 mol/L
- Quelles sont les conditions pour que le chlorure d'argent précipite à partir de la solubilité s ?
- Calculer alors la concentration en ions argent Ag+ pour que les ions Cl- précipitent ?
Merci d'avance
Attention, veuillez respecter les règles du forum : 1 exercice par topic...
Vous auriez mieux fait de faire un up dans votre demande du 10/01 "CONDITIONS DE PRÉCIPITATION DU CHLORURE D'ARGENT"
La réaction de précipitation s'écrit : Ag+(aq) + Cl-(aq)  AgCl(s).
AgCl(s).
Tant que [AgCl] 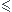 s la précipitation n'a pas lieu ; AgCl reste sous forme dissoute AgCl(aq).
s la précipitation n'a pas lieu ; AgCl reste sous forme dissoute AgCl(aq).
Comme 1 mol Ag+ donne 1 mol AgCl, la précipitation n'aura lieu que si [Ag+] > s
Ah oui oups je ferais atentions la prochaine fois.
D'accord j'avais une idée dans cette esprit mais du coup pour calculer la concentration en ions argent on fait comment ?
Toute valeur de concentration en Ag+ supérieure à s fera l'affaire.
Après, si on veut précipiter TOUS les ions Cl-, il faut connaître le volume de l'échantillon d'eau de Vichy testé et calculer la quantité d'ion Ag+ nécessaire en fixant arbitrairement, une concentration en ion argent.
Avez vous donné l'intégralité de l'énoncé ?
Oui j'ai fais un tp au préalable mais l'exercice est indépendant je pense je vais me débrouiller avec vos psites ,merci pour l'aide à bientôt
Bonjour pouvez vous aller voir mon sujet sur les techniques d'extraction et me venir en aide si possible. Merci d'avance
Bonsoir à vous deux,
@ lolojuju54 : tu n'es pas nouveau sur le forum, merci de faire plus attention la prochaine fois sur le respect des règles du forum


