Inscription / Connexion Nouveau Sujet
Titrage comprimé dibuprofène
Bonjour,
J'ai un énoncé d'exercice que je n'arrive pas a comprendre le raisonnement afin de trouver la réponse
Il faut que je détermine la masse m d'ibuprofène contenue dans le comprimé, à l'aide de cet énoncé
L'ibuprofène C13H18O2
(noté AH) est la substance active de nombreux médicaments de la classe des anti-inflammatoires non stéroïdiens.
On réalise le titrage de l'ibuprofène contenu dans un comprimé d'« ibuprofène 400 mg », contenant une masse attendue m/gp= 400 mg d'ibuprofène. Pour cela :
on réduit en poudre le comprimé dans un mortier ;
on sépare la molécule active des excipients (espèces chimiques inactives contenues dans le médicament) par dissolution dans l'éthanol que l'on évapore ensuite (les excipients sont insolubles dans l'éthanol) ;
on introduit la poudre obtenue dans un bécher et on ajoute environ 40 mL d'eau distillée.
Le titrage pH-métrique est effectué à l'aide d'une burette graduée contenant une solution aqueuse d'hydroxyde de sodium (Na+(aq), HO-(aq)) à Cb= (0,20  0,01) mol/L
0,01) mol/L
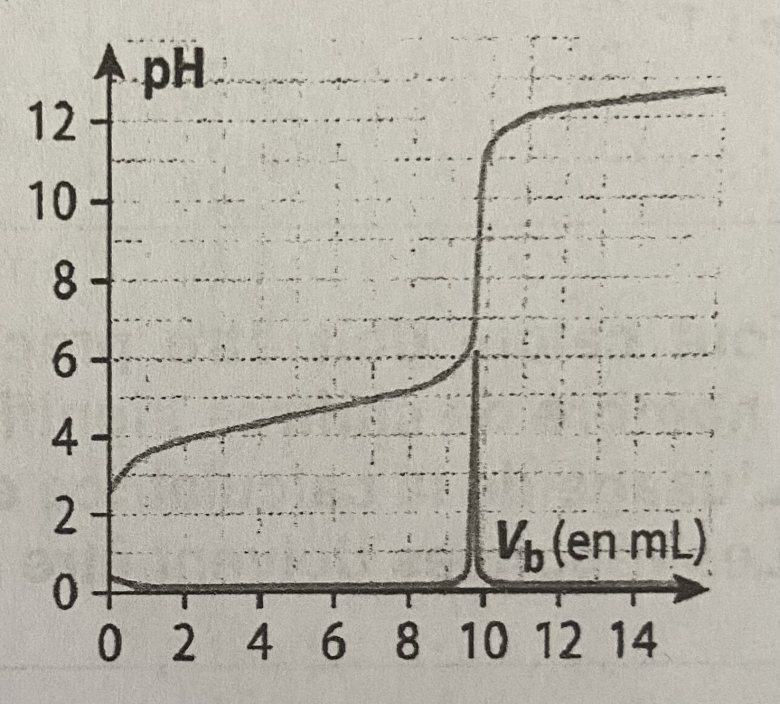
La courbe de titrage et sa dérivée sont présentées ci-dessous
Pouvez vous m'aider s'il vous plaît ?
Bonjour
Tu pourrais commencer par écrire l'équation de la réaction de l'ibuprofène (noté AH comme un monoacide faible) sur la solution d'hydroxyde de sodium.
Soit na la quantité de AH dans la solution dosée. Quelle est la relation simple entre na, Cb et le volume Vbe de solution d'hydroxyde de soium versé à l'équivalence.
Tu dois savoir comment repérer graphiquement Vbe...
Je te laisse réfléchir et proposer une solution. Pose si nécessaire des questions sur ce qui te bloque.
C'est cela. Reste à déterminer graphiquement la valeur VE[/sub du volume de solution d'hydroxyde de potassium. Tu pourras alors calculer la quantité n[sub]a d'ibuprofène puis, connaissant sa masse molaire, tu pourras calculer la masse.

 9,7
9,7
 Cb
Cb

