Inscription / Connexion Nouveau Sujet
titrage
Bonsoir, j'essaye de résoudre cet exercice :
Un échantillon de 0.500g est prélevé dans un mélange homogène d'hydroxyde de sodium et de chlorure de sodium. Cet échantillon est dissout dans l'eau distillée et titré. Le titrage indique qu'il faut ajouter 25,0 ml d'une solution d'acide chlorhydrique 0,200M pour neutraliser le NaOH contenu dans cet échantillon. Calculer le pourcentage en masse de NaOH dans le mélange.
La réponse est 40%.
j'ai écrit l'équation de réaction : NaOH + NaCl + HCl --> 2 NaCl + H2O
j'ai ensuite calculé la quantité de matière de HCl qui est 0,005 et maintenant je ne sait pas comment continuer.
Merci d'avance
Bonjour,
As tu fait un tableau d'avancement de la réaction ? Ca pourrait peut-être déjà t'aider à y voir plus clair 
Ensuite, tu nous dis qu'il faut une certaine quantité de matière d'acide pour neutraliser NaOH, il n'y a pas un terme qui commence et qui finit par un e qui caracterise cette notion, les propriétés qui en découlent peuvent peut-être nous avancer!
Par contre qui est M quand tu écris:" une solution d'acide chlorhydrique à 0.200 M", pareil la quantité de matière de HCl c'est en quoi en moles j'imagine mais ça pourrait être en mmol par exemple...
Bonjour, oui le voici (désolé ce n'est pas super propre)
par contre, je ne vois pas de quel terme on parle lorsque l'on veut neutraliser le NaOH. Je sais qu'il ne doit plus y avoir de NaOH dans la réaction finale mais je ne sais pas quel mot représente ceci.
"M" représente le "mol/L" d'une concentration. Ils le représentent comme cela lors de l'examen.
oui la quantité d'HCl trouvé est en mol, désolée j'ai oublié de le mentionner.
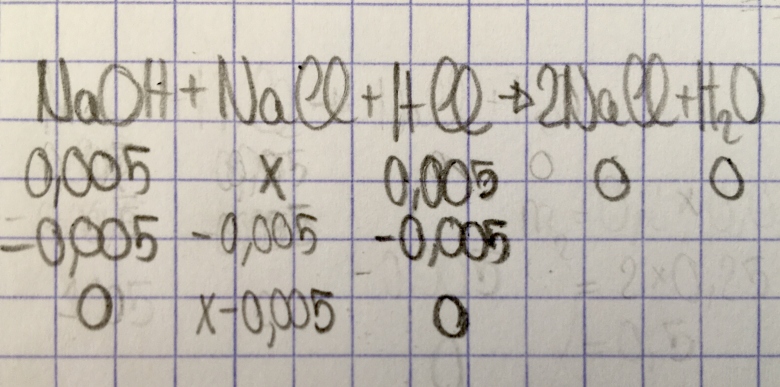
J'ai trouvé !
j'ai calculé la masse de NaOH qui ce trouve dans le mélange :
m=n*M =0,005*40 = 0,2
et donc le pourcentage en masse de NaOH dans le mélange de 0,5g est :
0,2/0,5 = 0,4 donc 40%


