Inscription / Connexion Nouveau Sujet
tableau d'avancement et calcul de PH
Bonjour, j'aurais besoin d'aide sur cet exercice, j'ai du mal avec les tableaux d'avancement.
On dissout un sachet de 1 000 mg d'aspirine (ou acide acétylsalicylique) de formule C9H8O4 dans de l'eau pour obtenir 500,0 mL de solution.
L'équation de la réaction qui modélise la transformation entre l'aspirine et l'eau est :
C9H8O4(s) + H2O(l) ↔ C9H7O4-(aq) + H3O+(aq)
1. Écrire les couples acide/base qui interviennent.
2. En considérant la réaction totale, déterminer l'avancement maximal xmax. En déduire la valeur finale de pH de la solution.
3. En réalité, le pH de la solution est de 2,9. Calculer alors la valeur xf de l'avancement final de la réaction.
4. Comparer xf et xmax puis conclure.
Donnée : M(C9H8O4) = 180,0 g.mol-1
mes réponses :
1) C9H8O4/C9H7O4- et H3O+/H2O
Bonjour, je n'arrive pas vraiment a le faire et je sais pas remplacer les valeurs littérale par les vrai valeurs
Si tu ne proposes rien je n'ai pas de point de départ pour t'aider.
Les tableaux d'avancement sont au programme de première.
Tu peux, au besoin consulter cette fiche --> ![]() [lien]
[lien]
Pour déduire la valeur finale de pH de la solution il faut que je fasse le tableau ? sinon je peux utiliser la formule pH = -log ([H3O+]) et pour trouver la c de H3O+ je fais c = m/V donc c = 1/0.5 = 2 (j'ai converti jsp si c'étai nécessaire) et mtn que j'ai la c j'applique la formule du pH donc -log(2) =-0.3 sauf que le pH ne peut pas etre negatif du coup je sais pas vraiment où je me suis trompé
Il ne s'agit pas d'appliquer des "formules" au hasard !
Essaie de compléter le tableau d'avancement ci-dessous.
A ton avis que représente n0 dans ce tableau ?
n0 représente la quantité initiale de C9H8O4
pour trouver n0 je dois appliquer la formule n = m/M
n = 500.0/180
n =2.8 mol
je met ca dans le tableaux ?
n0 est bien, en effet, la quantité de matière initiale d'aspirine C9H8O4.
Le calcul de la valeur numérique n'est pas prioritaire, mais tu peux, si tu le préfères le faire dès maintenant.
Appliquer une "formule" nécessite de bien connaître la signification des différentes termes de cette formule.
Ici on a n0 ( en non "n" ) qui est égal à m / M
Que représente " m " ? Quelle est sa valeur ? son unité ?
Mêmes questions pour " M "
m représente la masse elle est exprimé en gramme et sa valeur c'est 1 (j'ai convertie 1000mg en g)
M représente la masse molaire, elle est exprimé et en g.mol^-1 et sa valeur c'est 180g.mol
"m" représente en effet la masse ( la masse de quoi ? )
Sa valeur n'est pas de " 1 " mais de 1g ce qui n'est pas du tout la même chose.
M représente la masse molaire ( de quoi ? )
Sa valeur n'est pas de 180 g.mol mais de 180 g/mol et là encore ce n'est pas la même chose.
Compte tenu de ces données quelle est la valeur de n0 ?
"m" représente la masse de l'aspirine
M représente la masse molaire de C9H8O4
La valeur de n0 est 5.5x10^-3 mol
Nous sommes d'accord :
n0 = 5,6 . 10-3 mol
Il faut maintenant revenir au tableau d'avancement et le remplir soit littéralement ( ce qui est préférable ) soit à l'aide de la valeur numérique que tu viens de trouver.
Au sujet de ton tableau :
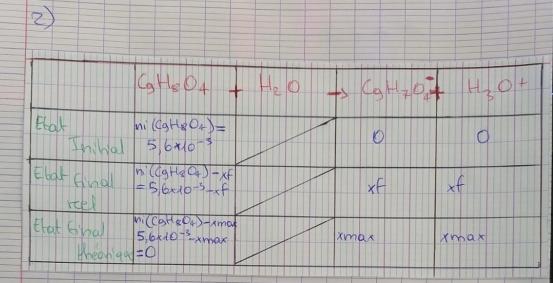
La ligne "état initial" n'appelle pas à plus de commentaires, sauf peut être à remarquer que ce que tu appelles ni(C9H8O4) n'est rien d'autre que ce qui a été noté par n0 précédemment.
La ligne Etat final réel sera utile pour répondre à la question 3
La ligne Etat final théorique est celle à utiliser pour répondre à la question 2
On est ici dans l'hypothèse (théorique) que la réaction étudiée est totale c'est à dire qu'elle se poursuit jusqu'à disparition totale du réactif limitant ( l'aspirine)
d'accord merci, mtn je dois remplir la ligne "etat final theorique" je dois donc calculer xmax, comme s'est dit dans l'énoncé je considéreque la réaction est totale et que donc l'acide (l'aspirine) est le réactif limitant. donc 5.6x10^-3 -xmax = 0
xmax = 5.6x10^-3 mol
c'est bien ca ?
Oui, c'est exact.
Reste pour terminer cette question 2 à calculer le pH de la solution correspondant à cet état final théorique.
voila ce que j'ai fais , est-ce correct ?
pour la qst 3 je dois calculer la valeur de xf reel grace au donné de l'énoncé, ici le pH.
d'apres le tableau d'avancement , nf (C9H8O4) = xf
avec le pH on trouve [H3O+] avec la formule : [H3O+] = 10^-pH = 10^-2.9 =1.3x10^-3 mol/L
xf = [H3O+] x V xf = 1.3x10^-3 x 0.5 (j'ai converti 500.0mL en L) =6.5x10^-4
xf = 6.5x10^-4 mol
** image supprimée **
Question 3 :
J'ai obtenu :
xf = [H3O+] * V = 10-pH * V = 10-2.9 * 0,5 = 6,3 . 10-4 mol
Question 2 :
Il me semble que tu as confondu n(H3O+) avec [H3O+]
Attention : Le règlement de ce site ne t'autorise pas à exposer ton travail sous forme d'images. (tableaux tolérés)
ah d'accord désolé, pour mon erreur de l'exo 2 je dois trouver la c de H3O+ pour pouvoir appliquer la formule du pH du coup je fais C = n/V ? donc 5.6x10-3/0.5 =0.01 et ensuite je fais la formule du pH
pH = 2
est-ce correct ?
[u]Question 3 [/u]:
J'ai trouvé
n(H3O+) = xmax = 1/180
[H3O+] = n(H3O+) / V= 1/(180 * 0,5)
pH = - log [H3O+] = -log (1/(180 * 0,5) = 2,0




