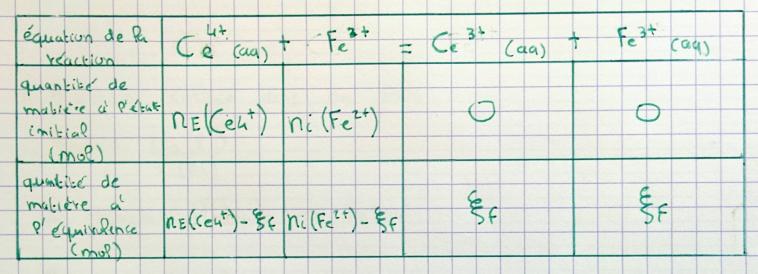Inscription / Connexion Nouveau Sujet
Tableau d'avancement à la demi-équivalence
Bonjour,
Je prépare mon TP sur un titrage d'oxydoréduction par potentiométrie : Le titrage d'une solution de sulfate de cérium (IV) par le sel de Mohr
Mais je bloque sur cette question :
- Etablir le tableau de bilan de matière à l'instant correspondant à la demi-équivalence. On désigne par nDE(Ce4+) la quantité de matière d'ions Ce4+ versée à cet instant et par VDE le volume correspondant
Je sais que la demi-équivalence est l'état où l'on a versé la moitié du réactif titrant nécessaire, mais je ne vois pas comment construire le tableau...
Pour l'instant j'ai juste le tableau d'avancement à l'équivalence
Bonjour.
A l'équivalence, les réactifs ont été mélangés en proportions stoechiométriques.
On a alors : nE(Ce4+) - xE = 0 et ni(Fe2+) - xE = 0
On tire alors : xE = nE(Ce4+) = ni(Fe2+)
Si Co désigne la concentration de la solution oxydante d'ion cérium(IV), on en déduit :
Co VE = ni(Fe2+)
A la demi équivalence, VDE = 1/2 VE et nDE(Ce4+) = Co VDE = Co  1/2 VE
1/2 VE
Soit encore : nDE(Ce4+) = 1/2 Co VE
C'est à dire finalement : nDE(Ce4+) = 1/2 ni(Fe2+)
Dans le tableau d'avancement, on a alors :
-pour les ions cérium((IV)
nDE(Ce4+) - xDE = 0 puisque l'ion cérium(IV) est le réactif limitant  xDE = nDE(Ce4+) = 1/2 ni(Fe2+)
xDE = nDE(Ce4+) = 1/2 ni(Fe2+)
-pour les ions fer(II)
nDE(Fe2+) = ni(Fe2+) - xDE
ce qui donne enfin : nDE(Fe2+) = ni(Fe2+) - 1/2 ni(Fe2+) = 1/2 ni(Fe2+)
Vous n'avez plus qu'à placer tout ceci dans le tableau d'avancement.
Au revoir.