Inscription / Connexion Nouveau Sujet
T.P. [Dosage par étalonnage de la salinité d'une eau de mer]
Bonsoir à toutes et à tous,
Je me présente ici, (actuellement en Terminale S) sur ce site car comme vous pouvez sûrement vous douter, je bloque complètement sur ce T.P de Spécialité Physique-Chimie sur l'EAU.
Je vais mettre deux liens qui correspondront aux "images" de mon T.P sous forme JPEG que voici :
** image de l'énoncé scanné effacée **
Tout d'abord, merci d'en avoir pris connaissance. Je bloque très exactement à la question "3. Calculer la salinité « s » de chaque eau de mer en g.mol-1 puis en UPS (unité définie dans le document précédent)." ainsi qu'aux suivantes (jusqu'à la partie "Détermination de la salinité de l'eau de mer artificielle par une méthode simple.") étant donné que le protocole expérimental a été réalisé en cours.
Je ne dois, cependant pas faire la partie "Préparation de l'eau de mer artificielle" car nous n'avons pas eu le temps de réaliser le protocole expérimental correspondant.
Pour la question 3. , je sais seulement cette formule : "S = 1,80655 Cl" mais je ne vois pas comment l'exploiter, sinon je pensais à utiliser la Concentration massique (Cm = m/V) mais encore une fois je ne vois pas du tout comment l'exploiter.
Je vous remercie d'avance pour votre éventuelle aide car cela fait déjà 2 jours que je bloque dessus.
Sur ce bonne fin de soirée,
Cordialement,
DT4ever.
Edit Coll : si tu veux de l'aide, merci de faire l'effort de recopier ton énoncé sur le forum 
![]()
Voici l'énoncé recopié de mon T.P (vous trouverez mes problèmes rencontrés dans le message précédent) :
Protocole expérimental
Préparation des solutions pour réaliser la courbe d'étalonnage
Préparer un volume V0 = 100 mL de solution aqueuse de chlorure de sodium de concentration molaire c0 = 5,0.10-2 mol.L-1. Il faut calculer la masse de chlorure de sodium NaCl à dissoudre.
Préparer, à partir de cette solution mère, une des cinq solutions filles présentées dans le tableau suivant : Solution fille Volume à préparer Concentration désirée Volume de solution mère à prélever
S1
V1 = 50 mL
c1 = 2,5.10-2 mol.L-1
S2
V2 = 50 mL
c2 = 1.10-2 mol.L-1
S3
V3 = 50 mL
c3 = 5.10-3 mol.L-1
S4
V4 = 50 mL
c4 = 2.10-3 mol.L-1
S5
V5 = 50 mL
c5 = 1.10-3 mol.L-1
Il faut calculer le volume de solution mère à prélever pour préparer chaque solution fille.
Mesures de conductivités
On étalonne le conductimètre.
Placer les 2 solutions préparées (la solution mère et la solution fille) dans des béchers.
Mesurer la conductivité des 2 solutions en prenant soin de bien rincer l'électrode entre chaque mesure, et en allant de la solution la moins concentrée à la solution la plus concentrée.
On mesure la conductivité de chaque échantillon d'eau de mer après les avoir dilués 100 fois.
Détermination de la concentration de l'eau de mer
1. Tracer la courbe d'étalonnage σ = f(c).
2. Modéliser, à l'aide d'une courbe de tendance, la relation entre la conductivité σ et la concentration « c » des solutions d'étalonnage.
3. Calculer la salinité « s » de chaque eau de mer en g.mol-1 puis en UPS (unité définie dans le document précédent).
Validation du résultat
4. Préciser quelles peuvent être les sources d'erreur.
Préparation d'une eau de mer artificielle et détermination par une méthode simple de sa salinité.
L'eau de mer contient de nombreuses espèces dissoutes, la majorité d'entres-elles sont sous forme d'ions. L'eau de mer de référence appelée « eau de mer normale » à la température de 15°C et à la pression atmosphérique normale de 1,0 bar, possède une salinité S de 35 g.kg-1. La densité de l'eau de mer normale d est égale à 1,02597.
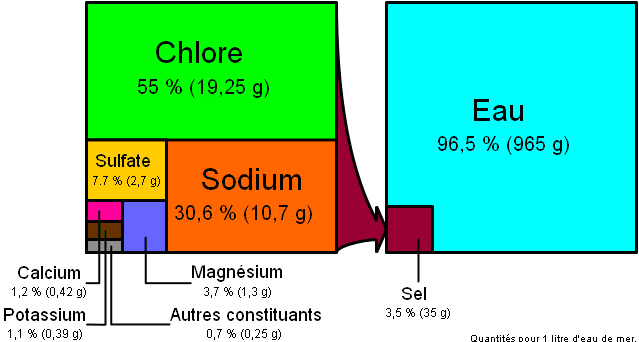
5. Quelle est la masse d'espèces dissoutes dans un m3 de cette eau de mer ?
(Voir schéma joint pour cette partie du T.P).
Détermination de la salinité de l'eau de mer artificielle par une méthode simple.
Lorsque l'on chauffe l'eau de mer, l'eau s'évapore mais les sels dissous restent dans le bécher et forment, en cristallisant, le « résidu à sec ». La masse du résidu à sec obtenu pour un litre d'eau de mer évaporée correspond à la salinité en g.L-1.
Proposer et mettre en oeuvre une méthode simple.
Validation du résultat : Comparer, par un calcul d'incertitude relative, la valeur expérimentale de la salinité avec la valeur théorique. Conclure sur la validité du résultat.
Voilà vous avez l'énoncé, je vous remercie d'avance pour votre éventuelle aide en sachant que ce T.P est pour demain et que mon professeur ne répond pas à mes questions.
Cordialement,
DT4ever.
bonjour,
Ton travail dépend de documents qui ont été effacés,si bien que j'ai du mal à reconstituer les données que tu as et
la formule s=1,806655*Cl fait intervenir la chlorinité .(Cl dans la formule)
Celle-ci se détermine à partir d'un dosage des ions halogènes par le nitrate d'argent.Or ,cette étape ne semble pas faire partie de ton travail.C'est pourquoi je ne comprends pas comment tu peux utiliser la formule.
Il est possible que des approximations soient faites dans ce TP,mais je ne peux pas les deviner.


