Inscription / Connexion Nouveau Sujet
Suivi temporel d'une transformation chimique 1'
Bonjour à tous
J'ai un exercice merci beaucoup d'avance
étude cinétique de la réaction entre Al(s) et
( H3O+(aq) + Cl- ( aq))
À l'instant t= 0 , on introduit une masse m = 0,54 g d'Aluminium Al( s ) dans un ballon contenant
V = 50 mL d'une solution d'acide chlorhydrique ( H3O+
(aq) + Cl-
( aq)) de concentration 2,0.10-1mol.L-1.
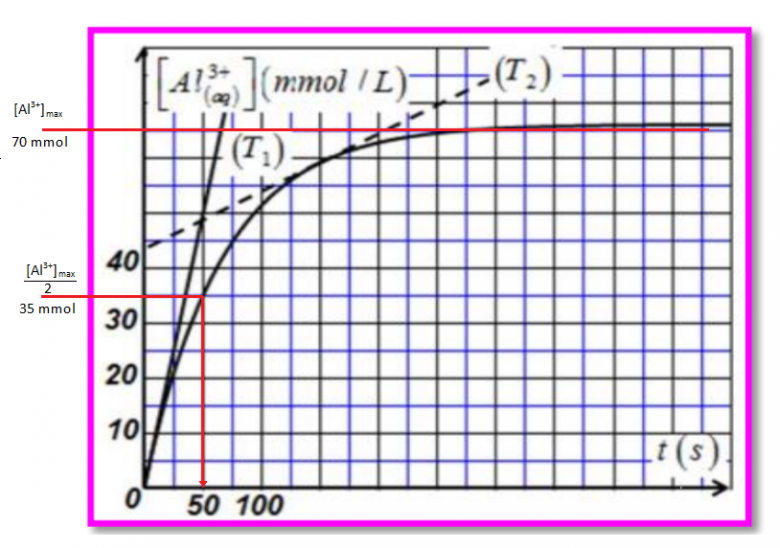
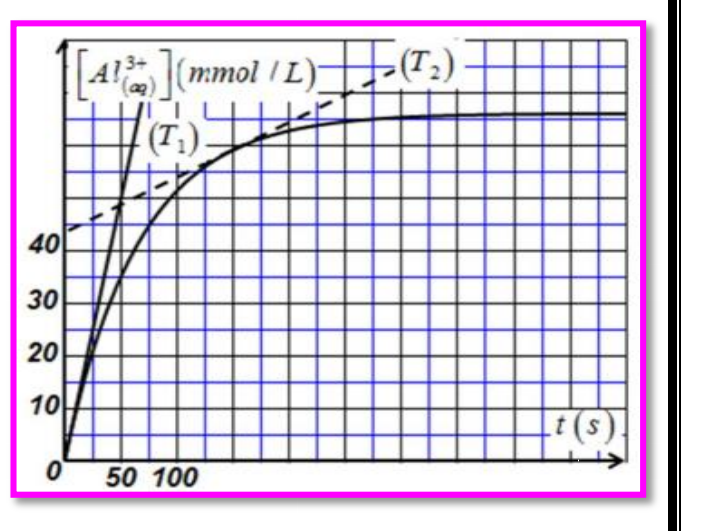
La courbe ci-contre représente la variation de la concentration en ion Al3+ dans le mélange
réactionnel au cours du temps ,
Données :
- La masse molaire atomique d'Aluminium est :
M ( Al ) = 27,0 g .mol-1
- Les couples mis en jeu sont :
H3O+(aq)/ H2(g) et Al3+ (aq) / Al(s)
- Toutes les mesures ont été prises à 20 ° C
1).Monter que l'équation bilan de la réaction
chimique étudiée s'écrit :
2 Al(s) +6 H3O+
(aq) -->2Al3+(aq) +3 H2(g) + 6H2O(l)
2)Citer une technique qui permet de suivre
l'évolution temporelle de cette réaction chimique. justifier votre réponse.
3).Calculer la quantité de matière initiale des réactifs
4).Dresser le tableau d'avancement.
5).Déterminer l'avancement maximal xmax et en déduire le réactif limitant.
6).en se basant sur le tableau d'avancement, trouver l'expression de l'avancement x (t) de la réaction à
l'instant t en fonction de [ Al3+]
7).Calculer la composition du système chimique à l'instant t = 75 s
8).Exprimer la vitesse volumique de la réaction chimique en fonction de [ Al3+]
9).Calculer la vitesse volumique de la réaction à l'instant t0 = 0 s
10).Comment évolue la vitesse volumique de la réaction chimique au cours du temps ? comment
interpréter cette évolution ? ( + interprétation à l'échelle microscopique : nombre de chocs efficaces)
11).Définir le temps de demi-réaction t1/2
12.Trouver qu'à l'instant t1/2 , on a [Al3+]t1/2=
et en déduire la valeur du temps de demi-
réaction t1/2
C'est à dire trouver [Al3+]t1/2
13).Comment peut-on accélérer cette réaction chimique ?
Mes réponses
1)
Couple H3O+/H2
3( 2H3O++ 2e-
--->H2(g) + 2H2O(l))
Couple Al3+/Al
2(Al3+(aq) + 3e-
<--- Al(s))
_____________________________
D'où l'équation bilan
2 Al(s) +6 H3O+
(aq) -->2Al3+(aq) +3 H2(g) + 6H2O(l)
2)on peut suivre l'évolution temporelle de cette transformation chimique par :mesure de pression car il y a un dégagement (formation) d'un gaz : H2(g)
3) ni(Al)=m/M=0,54/27=0,02mol
=2*10-2 mol
ni((H3O+)=C*V=2*10-1*50*10-3=10-2 mol
4)
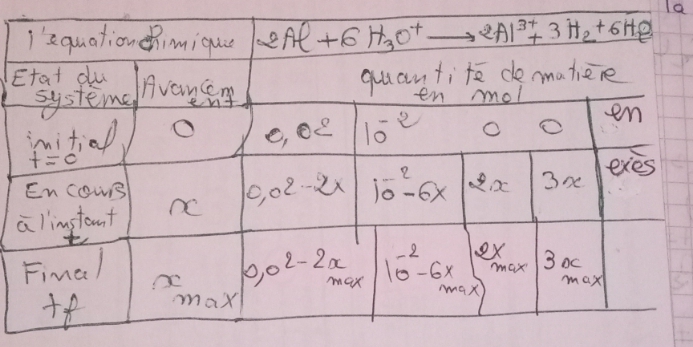
5) si Al est le réactif limitant , donc : 0,02-2xm=0
xm=0,01mol
Si H3O+ est le réactif limitant , donc 10-2-6xm=0
<=> xm=1,6*10-3 mol
le réactif limitant est la petite valeur ,d'où H3 O+ est le réactif limitant et xmax=1,6*10-3mol
6) on a d'après le tableau d'avancement :
[Al3+]t=
2x(t)=[Al3+]t*V
x(t)=
Merci beaucoup d'avance
Bonsoir,
Une lecture rapide à cette heure tardive me fait dire que ce que tu as fait me semble exact
Pour la question 2 : On peut en effet mesurer la pression du gaz à volume constant, mais il est plus commode de mesurer le volume gazeux à pression constante.
Bonjour
Merci beaucoup de m'avoir répondu !
7)La composition du système chimique à l'instant t=75s
D'après la courbe , à t=75s on a
[Al3+]t=75s=45mmol/L
Alors x(t=75s)=
=1125mmol=1,125mol
Pour Al
n(Al)t=75s=0,02*2x(t=75s)
=0,02-2*1,125= -2,23mol 
n(H3O+)t=75s=10-2-6x(t=75s)
=10-2-6*1,125
=-6,74mol 
n(Al3+)t=75s=2x(t=75s)=2*1,125=
2,25mol
n(H2)t=75s=3*x(t=75s)=3*1,125=
3,37mol
8)
9)
Merci beaucoup
Pour la question 10)
La vitesse volumique de la réaction chimique diminue avec le temps
Car la concentration des réactifs diminue au cours de la transformation chimique et la concentration des réactifs est un facteur cinétique
interprétation au niveau microscopique
Au cours de la réaction chimique , la concentration des réactifs diminue C=n/V
Alors le nombre de réactifs par unité de volume diminue ,donc le nombre de chocs efficaces décroit avec le temps et par conséquent la vitesse volumique de la réaction chimique diminue
Merci beaucoup à vous
Question 7:
Attention aux unités:
Les concentrations relevées sur le graphique sont en mmol/L
L'énoncé donne le volume de la solution en mL
Pour obtenir l'avancement cherché en mol il te faut exprimer les concentrations en mol/L et les volumes en L
Bonjour
Merci beaucoup à vous
La question 7 j'ai des erreurs de calculs
7)La composition du système chimique à l'instant t=75s
D'après la courbe , à t=75s on a
[Al3+]t=75s=45mmol/L=45*10-3 mol/L
Alors x(t=75s)=
=1,12*10-3mol
C'est juste ?
Merci beaucoup
Bonjour
Donc je rectifie ma réponse à la question 7)
7)La composition du système chimique à l'instant t=75s
D'après la courbe , à t=75s on a
[Al3+]t=75s=45mmol/L=45*10-3 mol/L
Alors x(t=75s)=
=1,12*10-3 mol
Pour Al
n(Al)t=75s=0,02-2x(t=75s)
=0,02-2*1,12*10-3
= 0,017 mol
n(H3O+)t=75s=10-2-6x(t=75s)
=10-2-6*1,12*10-3
= 3,28*10-3 mol
n(Al3+)t=75s=2x(t=75s)=2*1,12*10-3=
2,24*10-3mol
n(H2)t=75s=3*x(t=75s)=3*1,12*10-3=
3,36*10-3mol
Merci beaucoup
C'est bon.
Je trouve des résultats numériques légèrement différents parce que j'utilise pour les calculs une valeur non arrondie de l'avancement.
Bonjour
Merci beaucoup de m'avoir répondu
11)
Le temps de demi réaction est la durée nécessaire pour que l'avancement x soit égal à la moitié de sa valeur final xf , autrement dit , à l'instant t=t1/2 on a
x(t1/2)=xf/2
Si la réaction est totale , on a
Merci beaucoup
11)
Le temps de demi réaction est la durée nécessaire pour que l'avancement x soit égal à la moitié de sa valeur final xf , autrement dit , à l'instant t=t1/2 on a
x(t1/2)=xf/2
Si la réaction est totale , on a
Ce que tu as écrit est exact mais pourquoi s'arrêter en chemin ?
Question 12)
Déjà on a x(t)=
À l'instant t1/2 on a
x(t1/2)= (1)
À l'instant tf,on a x(tf)=
Soit xtmax= (2)
Diviser la 1er relation par la seconde relation 2
On obtient
Et puisque x(t1/2)=
D'où
D'après la courbe t1/2=25s
Merci beaucoup
Bonjour
Est ce que c'est juste ma rectification pour la question 9 ?
Est ce que j'ai donné une réponse incomplet pour la question 11 ?
Merci beaucoup
Question 9 : Je reprend ton post du 24-11-20 à 08:34
[quote]
9)
OK
Non l''unité reste la même : mol / L / s
Question 11 :
Tu as démontré (question 6) que la concentration en ions Al3+ est proportionnelle à l'avancement.
Il en résulte que lorsque l'avancement est égal à la moitié de sa valeur maximale, il en est de même pour la concentration en ions Al3+
Un simple coup d'il sur le graphique montre que la valeur maximale de la concentration en ions Al3+ est voisine de 70 mmol
A la date t1/2 cette concentration est donc voisine de 70/2 = 35mmol
Cela se produit à une date proche de 50s
t1/2  50s
50s
Bonjour
D'accord merci beaucoup à vous
J'ai trouvé t1/2≈46 s donc de 50s un peu près
Est ce que m'a réponse à la question 12 est juste ?
Merci beaucoup
Pour la Question 13)
On peut accélérer la vitesse de cette réaction , en augmentant la température du mélange réactionnel , puisque la température est un facteur cinétique.
Je n'ai pas vérifié le détail de tes calculs pour la question 12 mais le résultat que tu as obtenu est le même que celui que j'expose dans mon post du 24-11-20 à 17:37
Question 13 : OK
Bonjour
Merci beaucoup à vous
La question 12 est ce c'est juste pour la démonstration de l'expression ?
Merci beaucoup
Bonne journée
La question 12 est ce c'est juste pour la démonstration de l'expression ?
Je ne sais pas.
Je n'ai pas vraiment compris la signification de l'énoncé quand il demande :
Trouver qu'à l'instant t1/2 , on a [Al3+]t1/2=
Bonjour
D'accord merci beaucoup à vous
L'énoncé voulais dire :
"Trouver qu'à l'instant t1/2, on a
Merci beaucoup