Inscription / Connexion Nouveau Sujet
Structure des propriétés des matériaux
Bonjour,
J'aimerais de l'aide pour cet exercice car je comprends le problème mais je ne sais pas de quoi partir.
Enoncé : Déterminer le rendement de la saponification réalisée si on obtient une masse mexp = 11,8 g de savon.
Données : Formule du radical R de l'oléine : C17H33
Masse volumique de l'oléine :  oléine = 0,90 g/mL
oléine = 0,90 g/mL
Masses molaires : Moléine = 884 g/mol
MNa = 23,0 g/mol
MC = 12,0 g/mol
MH = 1,0 g/mol
MO = 16,0 g/mol
Le rendement d'une synthèse, noté  , sans unité, est égal au quotient de la quantité de matière en mole de produit obtenu, nexp, par la quantité de matière en mol de produit attendu, nmax :
, sans unité, est égal au quotient de la quantité de matière en mole de produit obtenu, nexp, par la quantité de matière en mol de produit attendu, nmax :  =
= .
Au préalable :
Je sais que n = .
Mais j'ai l'impression qu'il me manque quelque chose. J'ai fait un travail en classe avant cela mais ça ne me parle pas d'oléine alors je sais pas trop où chercher des informations. Merci d'avance pour votre aide.
Bonjour.
j'ai l'impression qu'il me manque quelque chose.
Revoyez donc votre cours ou furetez un peu sur Internet pour l'obtenir ; 133 000 résultats à la recherche "équation de saponification de l'oléine" !
A vous de jouer.
Ah oui, en effet, merci ! (Ci-joint l'équation de la réaction de saponification de l'oléine)
Je me dois donc de calculer :
3 x (17MC + 33MH + MC + 2MO + MNa) + (3MC + 8MH + 3MO)
qui est le résultat de la saponification réalisée.
Est-ce bien le cas ?
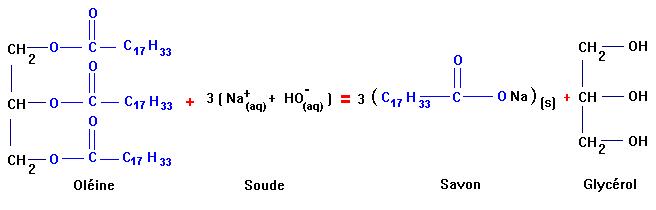
Je me dois donc de calculer :
3 x (17MC + 33MH + MC + 2MO + MNa) + (3MC + 8MH + 3MO)
Il faudra aussi s'intéresser au réactif limitant (sans doute l'oléine), et calculer la quantité de matière qui a été utilisée ; vous avez indiqué la masse molaire et la masse volumique, mais n'auriez vous pas oublié le volume ?
Affaire à suivre, je vais arrêter là pour le moment...
A plus.
Msavon + glycérol = 304 + 92 = 396 g/mol
n = m/M = 11,8/396 = 3,0.10-2 mol
Non, on me m'indique aucun volume dans mon énoncé.
Réactif limitant :
Hypothèse 1 : l'oléine est le réactif limitant
Hypothèse 2 : la soude est le réactif limitant
Seulement je n'ai ni la masse d'oléine ni la masse de soude pour calculer leurs quantités de matières respectives pour pouvoir déterminer lequel des deux est le réactif limitant... Que faire ?
Merci pour votre aide.
Msavon + glycérol = 304 + 92 = 396 g/mol
n = m/M = 11,8/396 = 3,0.10-2 mol
Les 11,8 g représentent la masse du savon, pourquoi rajouter le glycérol dans la calcul de la masse molaire ?
Non, on me m'indique aucun volume dans mon énoncé.
Donc n = 11,8 / 304 = 4,0.10-2
Désolée de l'erreur.
Dans la première partie on me dit 15 mL d'oléine... Mais il n'y a que ça alors qui semble se rattacher à cette deuxième partie. C'est pour ça qu'elle me semblait indépendante !
noléine = µoléine . Voléine / Moléine = 0,90 . 15 / 884 = 1,5.10-2 mol
avec µ la masse volumique de l'oléine en g/mL
V le volume d'oléine en mL
M la masse molaire de l'oléine en g/mol
n la quantité de matière en mol
Et désolée j'ai eu un problème avec LaTex c'est pour ça que mon calcul est écrit de cette manière.
n = 11,8 / 304 = 4,0.10-2
Dans la première partie on me dit 15 mL d'oléine
Vous avez bien calculé la quantité d'oléine qui a été utilisée, noléine = 1.53
 10-2 mol.
10-2 mol.
Revenez à l'équation de la réaction...
combien de mole de savon peut-on obtenir, théoriquement, à partir de 1 mol d'oléine ?
combien de mole de savon peut-on obtenir, théoriquement, à partir de 1.53
 10-2 mol d'oléine ?
10-2 mol d'oléine ?
Comparer ce résultat avec la quantité de savon effectivement obtenue en évaluant le rendement.
Allez, courage, c'est presque terminé !
Au revoir.
L'unité est la mole.
On peut en obtenir 3 mol de savon à partir de 1 mol d'oléine
On peut obtenir 3 . 1,53.10-2 = 4,59.10-2 mol de savon à partir de 1,53.10-2 mol d'oléine
nsavon = 4,0.10-2 < 4,59.10-2
Bonsoir Minisim,
Excusez-moi d'interférer mais par curiosité, comment introduisez-vous votre schéma du 26 sept 19h22 ?
Je ne suis qu'en 2nde.
Bonsoir Minisim,
Excusez-moi d'interférer mais par curiosité, comment introduisez-vous votre schéma du 26 sept 19h22 ?
Je ne suis qu'en 2nde.
<
Icône de l'image lors de la rédaction d'un message > choix du fichier sur votre PC ou DD externe, Clef USB... > insérer > *rédaction du message* > poster le message
Je comprends pas lequel est nexp et lequel est nmax
nexp correspond à la quantité de savon effectivement obtenue à l'issue de l'expérience :
nmax est la quantité de matière qui peut théoriquement être obtenue à partir d'une quantité d'oléine, noléine = 1.53
 10-2mol, dans l'hypothèse d'une réaction totale avec de la soude en excès.
10-2mol, dans l'hypothèse d'une réaction totale avec de la soude en excès.
OK ?
Du coup, comment on fait ? Désolée je suis perdue, je sais quel calcul faire mais je sais pas quel nombre mettre dedans  :?
:?
Vous pourriez m'éclairer un petit peu plus svp ?
Mais vous avez bien posé le calcul !!!
Par contre, il faut revoir votre calcul numérique et exprimer, comme c'est généralement l'usage, le résultat en %.
A vous.
Le rendement de la saponification réalisée est de 87 %.
Merci beaucoup pour votre aide. Bonne soirée 


