Inscription / Connexion Nouveau Sujet
Spectroscopie
Bonjour, j'ai un exercice à faire qui me pose soucis :
Les infusions de thé sont préparées à partir de feuilles de théier (Camelia Sinensis). Elles représentent, aujourd'hui, la deuxième boisson la plus consommée au monde, juste après l'eau plate. Parmi les constituants du thé, on retrouve la caféine (parfois appelée aussi théine, mais en réalité, ces deux noms désignent la même molécule).
Dans cet exercice, on s'intéressera à la caféine présente dans le thé et au nombre de tasses de thé qu'un adulte peut boire par jour sans risque pour la santé.
Données:
masse molaire moléculaire de la caféine : MCAF = 194 g.mol-1;
pour une personne en bonne santé, le risque d'intoxication à la caféine existe pour une consommation de plus de 400mg de caféine par jour pendant une durée prolongée.
1 Nombre de tasses de thé qu'un adulte peut boire par jour.
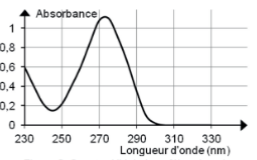
L'objectif est d'évaluer le nombre de tasses de thé du commerce qu'un adulte peut boire par jour sans risque pour la santé. Pour cela, on souhaite réaliser un dosage spectrophotométrique de la caféine présente dans une infusion de thé. Le spectre UV de la caféine obtenu après son extraction d'une infusion de thé par du dichlorométhane est donné (Cf figure 1).
1.1.Estimer la valeur de la longueur d'onde optimale à laquelle le spectrophotomètre pourrait être réglé pour réaliser les mesures d'absorbance lors du dosage. Justifier.
1.2.Sachant que le dichlorométhane est incolore et que l'absorbance de la caféine est quasiment nulle pour des longueurs d'onde supérieures à 330 nm, indiquer si la caféine est une espèce colorée dans le dichlorométhane.
On dissout de la caféine en poudre dans du dichlorométhane afin de préparer 100 mL d'une solution S0de caféine de concentration molaire C0= 5,7 × 10-4mol.L-1.
1.3.Déterminer la valeur de la masse de caféine qui a été dissoute dans le dichlorométhane afin d'obtenir 100 mL de solution S0.
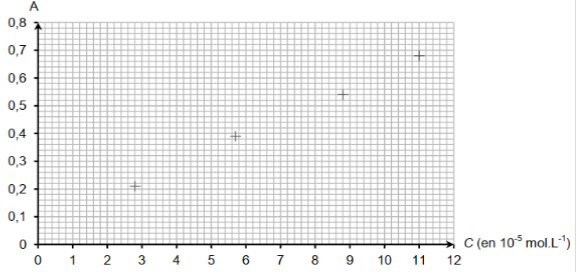
On prépare par dilution de la solution S0quatre autres solutions S1, S2, S3, S4dont on mesure l'absorbance à la longueur d'onde retenue (voir question 2.1.). Les mesures sont reportées sur le graphe de la figure 2.
1.4. Choisir, en justifiant la réponse, parmi les 4 lots de verrerie suivants, celui qui permet de préparer avec précision la solution S3 de concentration molaire en caféine égale à C3=5,7×10-5mol.L-1.
| Lot | 1 | 2 | 3 | 4 |
| Verrerie | Pipette jaugée de 2,0 mL Fiole jaugée de 20,0 mL | Pipette jaugée de 5,0 mL Fiole jaugée de 20,0 mL | Pipette jaugée de 10 mL Fiole jaugée de 20,0 mL | Pipette jaugée de 5 mL Fiole jaugée de 50,0 mL |
1.5.Une infusion de thé est préparée en introduisant un sachet de thé du commerce dans une tasse contenant de l'eau chaude. L'emballage conseille une durée d'infusion de deux minutes. Au bout de ces deux minutes, on retire le sachet et on laisse l'infusion de thé refroidir. La caféine de l'infusion est extraite à l'aide de 100 mL de dichlorométhane.On considère que la totalité de la caféine a été extraite par le dichlorométhane et qu'elle est contenue dans ce volume V=100mL.
Trop concentrée pour une mesure d'absorbance,la solution de caféine dans le dichlorométhane obtenue est tout d'abord diluée 10 fois. L'absorbance de cette solution diluée est mesurée à la longueur d'onde retenue (voir question 2.1.) et on obtient A= 0,43.
En se limitant au critère lié à la quantité de caféine, évaluer le nombre maximal de tasses de ce thé qu'un adulte pourrait boire par jour. Commenter.
1.1 La valeur de la longueur d'onde optimale devrait être 270 nm car c'est à cette longeur d'onde que l'absorbance est maximale.
1.2. C'est une espèce non colorée car elle n'absorbe pas des longueurs d'ondes du domaine du visible.
1.3. J'ai trouvé 1,1*10-2g.
1.4 C'est là que je bloque. Je sais que la quantité de matière de soluté est conservé lors d'une dilution.
C0*S0 = C3*S3.
Mais j'ai deux inconnus : S0 et S3 je ne sais pas comment les déterminer. J'arrive à par exemple S3=C0*S0/C3 mais je ne connais pas S0...
Bonjour,
Bonjour, j'ai un exercice à faire qui me pose soucis :
Pour avoir de l'aide, explique avec précision la nature de tes soucis.
"C0*S0 = C3*S3"
S0 est une solution, cela désigne l'objet, pas son volume ou sa concentration.
Donc plutôt "C0*V0 = C3*V3"
Vous avez bien en effet deux inconnues, mais vous connaissez le matériel à disposition (tableau), donc V0 V3 ne peuvent appartenir qu'à ce tableau.
Oui ils ne peuvent appartenir qu'à ce tableau mais comment je peux les calculer pour trouver la verrerie à utiliser ?