Inscription / Connexion Nouveau Sujet
Spectres RMN
Bonjour à tous,
En pleine révision pour le bac, je me suis aperçue qu'il y a quelque chose que je n'ai pas très bien compris à propos des spectres RMN.
En effet, dans l'un de mes exercices nous devions expliquer l'origine des différents signaux sur le spectre RMN de l'acide benzoïque.
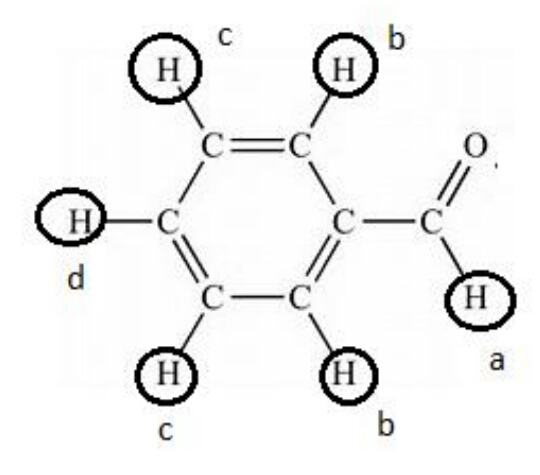
Voici la correction que nous a donné notre prof (les groupes de protons équivalents sont entourés sur la molécule ci-dessous).
Il y a 4 types de H équivalents, il y aura donc 4 signaux.
D'après la règle des « n+1 uplets »,
- Le H du groupe a n'a pas de voisin, le signal sera un singulet ;
- Les H de b présentent un voisin (Hc), le signal sera un doublet ;
- Les H de c présentent deux voisins (Hb et Hd), le signal sera un
triplet ;
- Le H de d présente deux voisins (les Hc), le signal sera un triplet.
Mais je n'ai pas compris pourquoi les 2 protons du b sont équivalents alors qu'il y en a un qui est plus proche de O que l'autre. De même, je n'arrive pas à comprendre pourquoi ceux des groupes c et d ne sont pas équivalents alors qu'il semble avoir le même environnement chimique ...
En espérant que quelqu'un pourra m'expliquer,
Merci d'avance. 
Bonsoir,
Ce n'est que sur ta feuille que l'un des protons "b" est plus proche de l'oxygène que l'autre.
En effet, le groupement -COH tourne en permanence autour de la liaison C-C qui le relie au cycle.
A cause de cette libre rotation, les 2 protons "b" sont à la même distance moyenne de l'atome d'oxygène.
Les protons "c" et "d" ne sont pas équivalents : L'un des deux est plus proche que l'autre du carbone du cycle qui porte le groupement -COH dont il est question ci-dessus



