Inscription / Connexion Nouveau Sujet
Solubilité s du chlorure de sodium dans l'eau (conductimétrie)
Bonsoir 
Alors voici un exercice bien complexe sur lequel je flanche! Cette histoire de solubilité m'ai totalment inconnue! alors voici l'énoncé:
Dans un bécher contenantenviron 100mL d'eau, on ajoute environ 50g de NaCl.
On agite pendant une heure.On constate alors qu'une partie du solide ne se dissout pas. On filtre et on récupére le filtrat.
On effectue une dilution au 1/1000 de ce filtrat pour obtenir une solution diluée de concentration c2.
La mesure de la conductance de la solution diluée donne G=780 microS
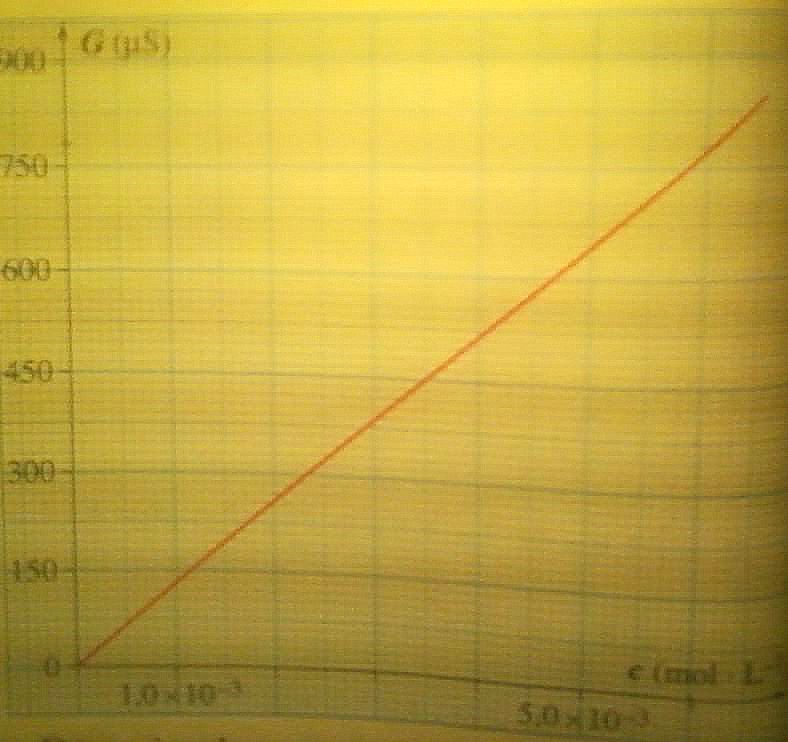
On a réalisé, d'autre part, la courbe d'étalonnage G=f(c) pour des solutions de chlorure de sodium.elle est fournie ci dessous:
a.détérminer la concentration c2 de la solution diluée
réponse: graphiquement 780 microS correspond à c2=6.0*10-3mol.L-1
b. En déduire la solubilité S(en mol.l-1)
C LA QUE JAI DES DIFFICULTEES: je pense que que je dois utiliser les formules de conductivités apprises, mais tout cela est peu explicite! Pourriez vous m'expliquer la démarche à appliquer, et me rappeler ce qu'est la solubilité?
Merci de votre aide  à bientot
à bientot