Inscription / Connexion Nouveau Sujet
RMN Proton
Bonjour, j'aurais besoin d'un coup de main SVP
On considère le spectre RMN du C4H7OCL
1) Comment déterminer les nombre de protons équivalents de chaque groupe avec la courbe d'intégration ?
2) Comment déterminer la formule développée de la molécule ?
Merci d'avance pour vos réponses !
Voici le spectre RMN : 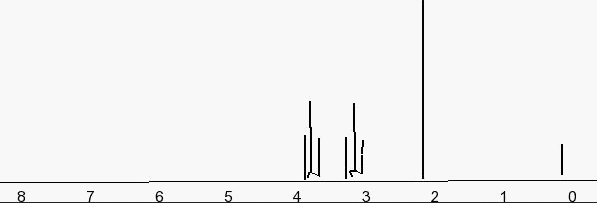
Edit Coll : image placée sur le serveur de l'  Merci d'en faire autant la prochaine fois !
Merci d'en faire autant la prochaine fois ! 
![]()
Bonjour Jordi20000 :
Je ne trouve pas ton spectre ?
Pour connaitre la hauteur d'un proton , tu mesures la hauteur totale de l'intégration en cm , puis tu divises cette hauteur par le nombre d'atomes d'hydrogène totaux .
Exemple : une molécule C4H10 , intégration totale 10 cm , la hauteur d'un proton sera de 1 cm . La hauteur de chaque palier divisé par 1 cm te donneras le nombre de H
par palier .
Bonnes salutations .
bonjour molécule,
pour trouver le spectre ,il faut cliquer "sur essayer image " et ensuite cliquer sur le petit spectre.
Je te laisse poursuivre tes explication qui sont très claires.
D'accord merci pour ton explication molécule 10 et comment peut-on déterminer les nombre de protons équivalents de chaque groupe avec la courbe d'intégration ?
Bonsoir Jordi20000 :
Ta molécule C4H7OCl doit être le 4-chlorobutane-2-one .
Le spectre montre 1 singulet à 2,1 ppm du CH3- ; 1 triplet à 3,4 ppm du -CH2-Cl ; 1 triplet à 3,8 ppm du -CO-CH2- .
Chaque -CH2- voisin voit ( 2+1 protons soit un triplet ) .
Bonnes salutations .
Merci pour ta réponse mais je n'ai pas trop bien compris
Est ce que tu pourrais m'expliquer ta démarche ?
Bonsoir Jordi20000 :
Regarde sur la publication la théorie de RMN ( règle n+1 page 16 ) ; se sera plus clair qu'une longue explication .
( http://www.cheneliere.info/cfiles/complementaire/chimie_organique_01/pdf/05_Spectroscopie_par_resonance_magnetique_nucleaire_(RMN_1H).pdf ) .
Bonnes salutations .
Merci enfaite j'ai compris Molecule10 dernière question et j'arrête de vous embêtez
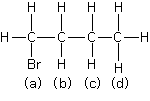
Comment est ce qu'on associe chaque proton a un signal sur le RMN comme ci-contre ?
Bonsoir Jordi20000 :
Il s'agit du 1-bromobutane : C4H9Br soit BrCH2-CH2-CH2-CH3 .
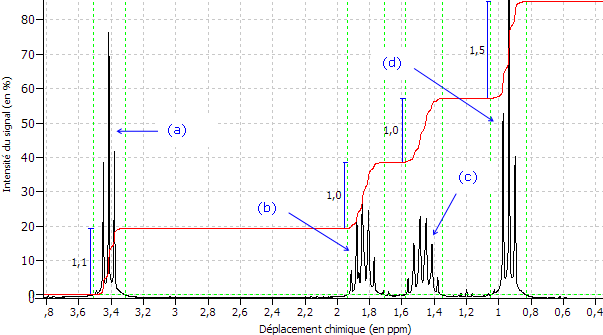
L'intégration totale du spectre correspond à ( 1,1+1+1+1,5 = 4,6 pour 9H ) ; 1H = 4,6 : 9 = 0,5 ( avec précision 0.51 ) .
A 3,4 ppm on trouve un triplet de 2 protons ( palier 0,55 x 2= 1,1 ) correspondant aux hydrogènes du -CH2-Br (a) qui couple avec le -CH2- ( b) voisin .
A 1,85 ppm on trouve un multiplet de 2 protons ( palier 0,5 x 2 = 1 ) correspondant aux 2 hydrogènes du -CH2- (b) qui couple avec les -CH2- voisins (a et c ) .
A 1,5 ppm on trouve un multiplet de 2 protons ( palier 0,5 x 2 = 1 ) correspondant aux 2 hydrogènes du -CH2- (c) qui couple avec le -CH2- voisin (b) et le CH3 (d) .
A 0,9 ppm on trouve un triplet de 3 protons ( palier 0,5 x 3 = 1,5 ) qui correspond au CH3 (d) qui couple avec le -CH2- voisin (c) .
La distance qui sépare chaques raies des signaux , s'appelle la constante de couplage mesurée en Hz ; elle est la même pour les 4 paquets de signaux .
Bonnes salutations .
Merci Molécule 10 enfait je viens de comprendre dernière question comment trouver le nombre de protons équivalents dans chaque groupe ?


