Inscription / Connexion Nouveau Sujet
Réaction suivie par conductimétrie.
Bonsoir, j'ai besoin d'aide pour une seule question Svp, car elle m'empeche de continuer mon exercice.
Le chlorure de tertiobutyle peut réagir avec l'eau selon la réaction d'équation (voir ci-dessous)
Le chlorure de tertiobutyle sera noté R-CL et l'alcool tertiobutylique R-OH.
Dans deux béchers différents préparer exactement le même mélange constitué d 30g d'eau et 20g d'acétone.
Placer un des béchers dans un bain a 30°C. Quand l'équilibre thermique est atteint plonger la cellule conductimétrique dans les béchers et mettre sous agitation. Ajouter alors 1ml de chlorure de tertiobutyle et déclencher l'enregistrement de la valeur de la conductivité de la solution en fonction du temps.
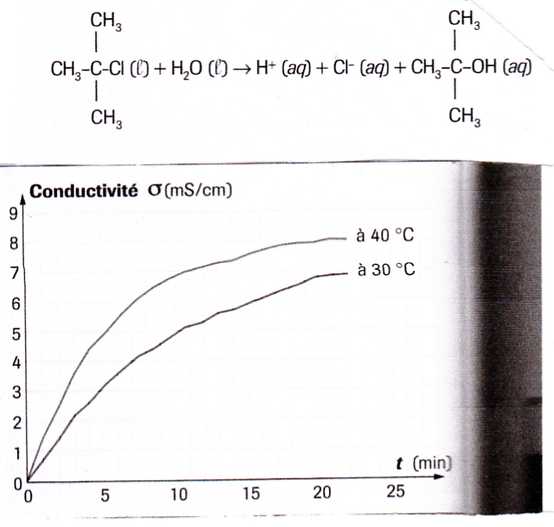
Pour chaque température l'étude est menée pendant 20 minutes. Les graphiques =f(t) sont donnés ci-dessous.
Données:
Densité du chlorure de tertiobutyle: 0.85
Massee molaire: 95.6g/mol
a) Calculer la quantité de matière initiale notée n0 de chlorure de tertiobutyle.
Pour cela j'ai fait:
d= R-Cl/
R-Cl/ eau
eau
<=>  R-Cl=0.85g/cm3
R-Cl=0.85g/cm3
De plus  R-Cl= m/M et
R-Cl= m/M et  R-Cl=n
R-Cl=n M/VR-Cl<=> nR-Cl=
M/VR-Cl<=> nR-Cl=
 V/M donc n=0.85
V/M donc n=0.85 0.001/92.6 = 9.179
0.001/92.6 = 9.179 10-6mol.
10-6mol.
Sauf que je ne sais pas si le volume est de 10 ml au total ou si c'est 1ml qui s'ajoute à chaque fois pendant 20 minutes donc 20 Ml ... ?
Merci de m'aider .
m= *V
*V
 =0,85g/cm3 V=1mL=1cm3
=0,85g/cm3 V=1mL=1cm3
m=0,85g
n=m/M=0,85/92,5= 9,19.10-3 mol =9,2.10-3mol (erreur de masse molaire dans l'énoncé).
on verse 1mL de tertiobutyle 1 fois et on mesure la conductivité (due aux ions Cl- et H+ )à diverses dates ,pendant 20min.

 Merci beaucoup!
Merci beaucoup!

