Inscription / Connexion Nouveau Sujet
Questions sur les proteines
Bonjour tous le monde , j'ai un exercice a faire pour mercredi et je ne comprend pas vraiment.. Alors si quelqu'un pourrez m'aidez cela serai très sympathique  .
.
Donc ,
1) Définir la liaison peptidique en prenant comme exemple l'alanine ( acide 2-aminopropanoique).
2) Trouver quelles seraient les proportions en C, H, O, N d'une protéine dont l'hydrolyse ne donnerait que de la glycine ( acide 2 -aminoéthanoique).
3) En notant 1 la glycine, 2 l'alanine et 3 la sérine ( acide 2-amino-3-hydroxypropanoique), écrire la structure primaire semi-développe d'une protéine dans laquelle on a a séquence 1-2-2-3.
J'ai donc fait :
1) liaison peptidique : Liaison entre le groupe amine (-NH2) d'un acide aminé et le groupe acide carboxylique (-COOH) d'un autre acide aminé.
2) C2H5O3N
3) Je ne comprend pas..
Pourriez vous me dire si ce que j'ai fait est bon et eventuellement m'aidez pour la question 3 Merci.
Salut  !
!
1) ok
2) ça me paraît correct
3) Tu enchaînes une glycine, une alanine, une alanine et une sérine. Tu écris ça en formule semi-développée
1) oui, c'est une réaction de condensation puisque tu perds une molécule d'eau comme suit :
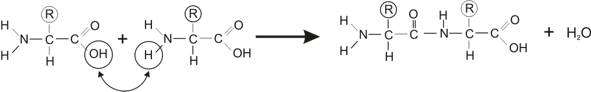
D'une manière générale je te conseille ce lien même s'il va te paraître plus complexe : ![]()
2) ce serait la formule de la glycine (directement). ici on te demande une molécule dont l'hydrolyse ne donnerait que de la glycine, cad une molécule qui après réaction avec l'eau, forme cette fameuse glycine
3) oui tu mets les peptides les uns à la suite des autres : tu formes ainsi un polypeptide


