Inscription / Connexion Nouveau Sujet
Produit de solubilité
Bonjour, il y a une question où je bloque
Voici l'énoncé :
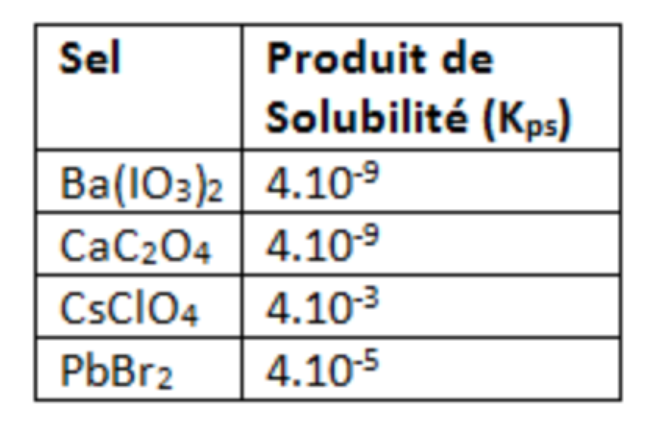
lequel des sels suivants possède la solubilité la plus petite ?
Je sais que c'est entre Ba(IO3)2 et CaC2O4 car ils ont tous les deux un produit de solubilité faible.
J'ai donc écris leur équation ionique :
Ba(IO3)2 -> Ba^2+ + 2(IO3)^2-
CaC2O4 -> Ca^2+ + C2O4^2-
mais après je bloque, je ne sais pas comment raisonner pour savoir lequel des deux a le produit de solubilité le plus faible..
Merci
Bonjour,
Attention, ta première équation de dissolution n'est pas équilibrée en charges électriques.
Il n'est pas toujours vrai que le plus petit produit de solubilité soit lié à la plus petite solubilité. Il est indispensable de tenir compte de la stoechiométrie de la réaction de dissolution.
Ici, en pratique il te faut calculer la solubilité des deux sels à partir de leur produit de solubilité et comparer les résultats.


