Inscription / Connexion Nouveau Sujet
problème de solubilité
Bonsoir,
Je ne comprends pas comment résoudre ce problème, pourriez-vous m'aider, s'ils vous plait?
Voici l'énoncé :
En admettant que la concentration en PO43- dans les os vaut 8,10.10-6 mmol.L-1, calculer la concentration minimale en Ca2+ nécessaire pour que la calcification des os ait lieu. (On considère qu'il se forme du Ca3(PO4)2) ? Kps = 1,00 10-25
a) 1,15.10-3 M
b) 1,15.10-4 M
c) 1,15.10-5 M
d) 1,15.10-6 M
e) 1,15.10-7 M
Merci d'avance.
Bonsoir,
Ecris l'équation de la réaction qui conduit à la formation du Ca3(PO4)2
A quelle condition portant sur les concentrations ioniques cette réaction pourra t'elle commencer à se produire ?
Bonjour,
Voici la réaction que j'ai écrite :
Ca3(PO4)2 = 3Ca2+ + 2PO4 3-
Je dirais que lorsque la concentration des ions dépasse Kps, la réaction commence à se produire.
En fait, la réaction de formation de Ca3(PO4)2 est la réaction inverse de celle que tu as écrite.
Mais on peut raisonner sur celle que tu as écrite qui est la réaction de dissolution de Ca3(PO4)2 .
Le produit ionique Q des concentrations est :
Q = [Ca2+]³ * [PO43-]²
et il se formera du Ca3(PO4)2 si Q>=Kps
L'énoncé te donne [PO43-] ainsi que Kps
Tu devrais donc pouvoir choisir la proposition correcte.
Mais je calcule Q et je trouve Q< Kps
Voici comment j'ai fait :
(8,10 * 10^-9 ) ^3 * (8,10*10^-9) ^2 = 3,48 * 10^-41 (< 1,00 * 10^-25)
Dans ce cas il n'y a pas de formation
Non.
Tu ne peux pas calculer Q, puisque [Ca2+] est l'inconnue que tu dois trouver !
Rappel : La question est " calculer la concentration minimale en Ca2+ nécessaire pour que la calcification des os ait lieu. "
L'inéquation à résoudre est : Q 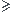 Kps
Kps
avec Kps = 1,00 . 10-25
[PO43-] = 8,10 . 10-9 mol/L
[Ca2+] 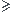 ? C'est ce qu'on te demande de calculer ( Voir le Rappel )
? C'est ce qu'on te demande de calculer ( Voir le Rappel )
D'accord, alors j'ai posé que S = SO4 3- = 8,10 * 10^-9 mol/L.
D'après l'équation, nous avons 3 Ca2+ et 2 PO4 3- .
Voici l'équation que j'ai écrite :
1,00 * 10^-25 = s^3 * s^2
1,00 * 10^-25 / (8,10*10^-9)^2 = 1,52 * 10^-9 mol/L = s^3
s = racine cubique de 1,52*10^-9 = 1,149 * 10^-3 mol/L.
Mon développement est-il correct?
Le bon résultat est [Ca2+] 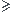 1,15.10-3 mol/L
1,15.10-3 mol/L
Sur le plan de la rigueur scientifique ton développement est une horreur.
Tu poses (ligne 1) que " s " = 8,10 * 10-9 mol/L
Et tu démontres à la dernière ligne que ce même " s " = 1,149 * 10-3 mol/L !
Tu sembles penser que les concentrations en ions Calcium et phosphate sont égales ce qui est faux.
La concentration en ions phosphate est donnée. La concentration minimale pour qu'il se produise une précipitation est à trouver.
Donc si ton " s " représente la concentration en ions phosphate, il ne peut pas représenter aussi la concentration en ions Calcium.
Pourquoi ne pas suivre tout bêtement mes indications du 28-05-19 à 23:59 ?


