Inscription / Connexion Nouveau Sujet
- Pourquoi les hydrocarbures ne sont-ils pas soluble dans l'eau
bonjour!
- Pourquoi les hydrocarbures ne sont-ils pas soluble dans l'eau ?!
merci de me répondre et je vous remercie d'avance
Bonjour,
un hydrocarbure possède des liaisons C-H.
D'après les tables, 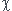 (C)=2.4 et
(C)=2.4 et 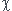 (H) = 2.1.
(H) = 2.1.
2.4-2.1=0.3<0.5 donc la liaison n'est pas polarisée donc la molécule est apolaire.
L'eau étant un solvant polaire (contrairement au cyclohexane), les hydrocarbures ne sont pas solubles dans l'eau. En effet,
-un composé polaire est soluble dans un solvant polaire,
-un composé apolaire est soluble dans un solvant apolaire.
C'est pourquoi les hydrocarbures ne sont pas solubles dans l'eau.


