Inscription / Connexion Nouveau Sujet
Pluies acides
Merci marcs 35 ,tu ma aider a terminer cette excercice, je voulais que tu m'aide juste une derniere fois pour ce dernier excercice ou je reste bloquer sur le 6, enfin si sa te derange pas.
Salut tout le monde j'aimerai bien qu'on m'aide pour le numeros 5,6 car je bloque sur ces numeros.
Les pluies sont naturellement acides à cause du dioxyde de carbone présent dans l'atmosphère.
De plus, la combustion des matières fossiles (charbon, pétrole et gaz) produit du
dioxyde de soufre et des oxydes d'azote qui amplifient ce phénomène d'acidification.
Lorsque les pluies s'écoulent des toits, elles sont recueillies par des gouttières métalliques
constituées de zinc.
Le zinc est un métal qui réagit en milieu acide selon la réaction d'équation : (dessin au -bas )
On considère le passage de 5 L d’eau acidifiée à raison d’une concentration en ion oxonium
:
[H3O ] = 1,0.10 mol.L
+ –4 –1 sur une gouttière de zinc de masse 500,0 g.
1 De quelle quantité initiale de zinc dispose-t-on ? (0,5 point)
2 De quelle quantité initiale d’ions oxonium dispose-t-on ? (0,5 point)
3 Construire un tableau de quantité de matière des espèces chimiques, faisant apparaître
l’avancement x. (1,5 point)
4 Quel est le réactif limitant ? Justifier la réponse. (1 point)
5 Quelle masse maximale de dihydrogène peut-on obtenir si le réactif limitant est entièrement
consommé à l’état final ? (0,5 point)
6 Quel volume de dihydrogène gazeux cette masse correspond-elle (à 25°C et à la pression
atmosphérique) ? (1 point)
Données : Masses molaires atomiques (en g.mol–1) : Zn : 65,4 ; H : 1,0.
Volume molaire VM d’un gaz à 25°C et à la pression atmosphérique : 24,0 L.mol–1.
Réponses :
1) 1) Il faut que tu trouve la quantité initiale de zinc
donc n(x)= m(x) / M(x)
- n(x) : quantité de matière en mol.
- m(x) : masse en gramme (m).
- M(x) : masse molaire en g.mol^-1.
500/65,4=7,65mol.
2)n(H3O^(+)=[H3O^(+)]*V=5*10^(-4) mol .
On dispose de 5,0.10-4 d'ions oxonium initialement, étant donné qu'il y a 5 litres d'eau et que la quantité d'ions oxonium pour 1 litre d'eau est de : 1,0 .10-4 .
3) (DESSIN AU - BAS ).
4)Si le zinc est le réactif limitant, alors il est totalement consommé donc n(Zn)i - xmax = 0 alors xmax= n(Zn)i = xmax == 7,65 mol .
Si l'ion oxonium est le réactif limitant alors n(H3O+)i - 2xmax = 0, soit xmax =n(H3O+)i/2 = 5,0 X 10-4/2 = 0,00025 = 25.10-5 mol.
Le réactif limitant est l'ion oxonium car il conduit à la valeur de l'avancement maximal la plus faible, xmax = 25.10-5 mol.
5)Il faut d'abord calculer le nombre de moles de H2 produit
L'équation bilan montre que n(H3O+)/2=n(H2)/1
Or on consomme 25.10-5 moles de n(H3O+),
donc on fabrique 25.10^-5/2=12,5 .10^-5 moles de n(H2)
6) Je bloque.
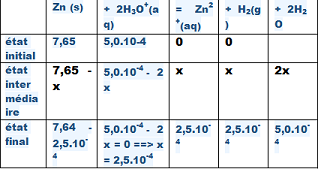
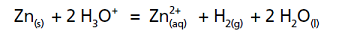
*** message déplacé ***
Edit Coll : titre modifié
Dans le tableau, sur la dernière ligne, il faut mettre xmax ou xfinal ou xf .
5 Quelle masse maximale de dihydrogène peut-on obtenir si le réactif limitant est entièrement
consommé à l'état final ? (0,5 point)
La réponse de la 5 est inexacte pour 2 raisons :
1) on demande une masse, pas une quantité de matière
2) la quantité de matière est inexacte
La quantité de matière de dihydrogène se lit directement dans le tableau

La masse molaire du dihydrogène étant égale à 2 g, on a donc une masse de dihydrogène égale à
 2,5.10-4 )
2,5.10-4 )
Question 6
A 25°C et à la pression atmosphérique, le volume molaire est de 24,0 L.mol-1
Donc le volume de dihydrogène est :
*** message déplacé ***
Annaelle >>
Il me semble que tu prends de plus en plus de libertés avec les règles du forum. Par exemple, tu postes de plus en plus de réponses sous forme d'images en faisant du copier-coller d'éléments que tu trouves ici ou là. Cette fois-ci tu ne respectes pas une règle qui permet d'avoir des topics ne traitant que d'un seul problème.
Je te conseille vivement de (re)lire les règles de ce forum et de les appliquer si tu veux pouvoir continuer à y venir te faire aider.
Mode d'emploi du forum 
![]()
Les questions fréquentes liées à l'utilisation des forums 
![]()
Clique sur les maisons, ce sont des liens !


