Inscription / Connexion Nouveau Sujet
physique nucléaire
Bonjour à tous,
Je suis face à un léger soucis, car il se trouve que je suis bloqué à un exercice de physique nucléaire.
Voici l'énoncé : Calcule, en MeV, l'énergie libérée au cours de la réaction nucléaire suivante.
Réaction : 2^H + 2^H -> 3/2^He + 1/0n
A 2 2 3 1
Z 1 1 2 0
Ma réponse :
Formule utilisé -> noyaux fils - noyaux pères
Max - Zme = 2 - 1.0,0005
= 1,9995
Max - Zme = 3 - 2.0,0005
= 2,999
Max -Zme = 1 - 0.0,0005
= 1
Ensuite :
A partir de là je me perd un peu.
La suite de ma résolution chaotique :
2,999 - 3,999 ( 1,9995+1,9995) = -1 uma
Ensuite si la réponse est juste j'effectuerais une conversion du uma en kilo pour ensuite introduire la valeur dans la formule de l'énergie de liaison puis de J convertir en MeV.
Je vous remercie d'avance pour votre ou vos aides  !
!
Bonnes vacances.
Il faut prendre les masses atomiques avec beaucoup plus de précision ...
Et il ne faut pas non plus commettre l'erreur classique trop souvent vue d'utiliser les masses des atomes au lieu des masses de leur noyaux.
Masse du NOYAU de H(1,2) = 2,013552 u
Masse du noyau de He(2,3) = 3,014929 u
Masse d'un neutron : 1,008666 u
Delta m = 3,014929 + 1,008666 - 2 * 2,013552 = -0,003509 u
Delta m = -0,003509 * 1,66054.10^-27 = -5,8268.10^-30 kg
E = Delta m * c² = -5,8268.10^-30 * 299792458² = -5,2369.10^-13 J
E = -5,2369.10^-13/(1,602.10^-13) = -3,27 MeV (le - signifie que la réaction fournit de l'énergie au "monde extérieur")
Ce résultat peut être vérifié sur ce lien : ![]()
On y voit ceci :
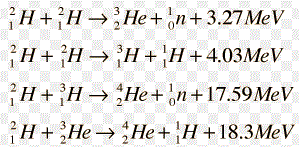
Sur certains sites (et aussi souvent dans les exercices scolaires), on voit souvent un autre résultat ... qui est FAUX.
Il provient du fait de confondre les masses des noyaux avec les masses des atomes.
Sauf distraction. 
Bonsoir,
Je vous remercie beaucoup pour votre explication ! 😊
Il y a juste une chose qui me trotte dans la tête. Ma professeur, durant les interros nous donnes pas toujours la masse atomique. Alors à partir de là faut-il que je prenne en compte juste les données donner ?
Merci encore de votre aide.
Bonne soirée.
Pour des calculs d'énergie sur de la fission ou de la fusion nucléaire, on doit partir les masses très précises (ou parfois des énergies de liaison atomique).
Soit le prof fournit ces masses, soit on est sensé les trouver sur le net.
Dans les 2 cas, il y a souvent des erreurs (par le prof ou le net d'ailleurs).
Il y a des sources plus fiables que d'autres.
Une des mieux faites est celle de wiki ... à condition de choisir les bonnes, c'est à dire celles sur les isotopes de l'élément cherché.
Exemple : pour le deuterium, aller voir sur wiki dans les isoopes de l'hygrogène. ![]()
Tu y trouveras par exemple pour le deuterium (H1,2) : masse isotopique = 2,0141017778 u
MAIS ATTENTION, ces masses sont TOUJOURS celle de l'atome. Pour trouver la masse du noyau, il FAUT donc retirer la masse des électrons.
La masse de l'électron est de 0,000549 u
Pour le deuterium, il y a un seul atome (puisque c'est de l'hydrogène) et donc la masse du noyau de deuterium est : m = 2,0141017778 - 0,000549 = 2,013553 u
C'est la masse à prendre en considération pour le noyau de deuterium.
Pour de He(2,3), aller voir sur wiki à isotope de l'helium : ![]()
On y trouve ceci : masse du (He 2,3) = 3,0160293191 u (cà c'est pour l'atome)
Et pour avoir la masse du noyau, il faut ici soustraire la masse de 2 électrons ...
Il y a d'autres sources fiables, mais celles indiquées ci-dessus suffisent presque toujours.
Se méfier des sources (surtout scolaires) ... très souvent, il est indiqué masses des noyaux ... et ce qui suit est la masse des atomes et souvent aussi c'est complètement faux. Eu un mot, c'est le foutoir.
Remarques:
Si les calculs ne concernent pas des réactions de fission ou de fusion nucléaires, la connaissance des masses atomiques avec beaucoup de précision est en général non utile.



