Inscription / Connexion Nouveau Sujet
nucleaires
SALUT TOUT LE MONDE,SVP
J'AI BESOIN UNE IDEE POUR LA LDERNIERE QUESTION,MERCI DABORE
Le noyau de sodium 11𝑁a(A=24)
se désintègre spontanément en noyau de magnésium 12
24𝑀𝑔 avec
production d'une particule 𝑋.
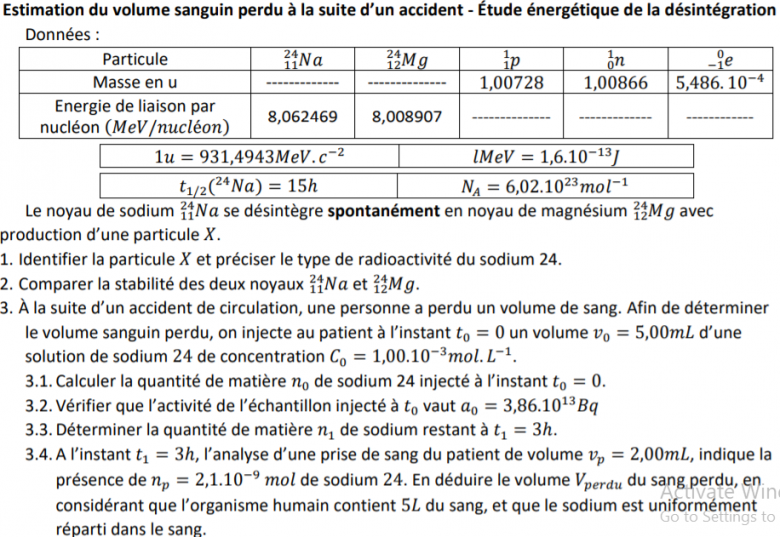
1. Identifier la particule 𝑋 et préciser le type de radioactivité du sodium 24.
2. Comparer la stabilité des deux noyaux 11𝑁
24 𝑎 et 12
24𝑀𝑔.
3. À la suite d'un accident de circulation, une personne a perdu un volume de sang. Afin de déterminer
le volume sanguin perdu, on injecte au patient à l'instant 𝑡0 = 0 un volume 𝑣0 = 5,00𝑚𝐿 d'une
solution de sodium 24 de concentration 𝐶0 = 1,00.10
−3𝑚𝑜𝑙. 𝐿
−1
.
3.1. Calculer la quantité de matière 𝑛0 de sodium 24 injecté à l'instant 𝑡0 = 0.
3.2. Vérifier que l'activité de l'échantillon injecté à 𝑡0 vaut 𝑎0 = 3,86.10
13𝐵𝑞
3.3.Déterminer la quantité de matière 𝑛1 de sodium restant à 𝑡1 = 3ℎ.
3.4. A l'instant 𝑡1 = 3ℎ, l'analyse d'une prise de sang du patient de volume 𝑣𝑝 = 2,00𝑚𝐿, indique la
présence de 𝑛𝑝 = 2,1.10−9 𝑚𝑜𝑙 de sodium 24.
En déduire le volume 𝑉𝑝𝑒𝑟𝑑𝑢 du sang perdu, en
considérant que l'organisme humain contient 5𝐿 du sang, et que le sodium est uniformément
réparti dans le sang.
POUR LES QUESTION PRECEDENTES;
1 B-
2 NA PLUS STABLE QUE MG (IL NOUS DONNE LES ENERGIE DE LAISON SOUS PAR NUCLEAONS FORME DE TABLEAU)
3.1 5*-6 MOL
3,2 3.863*1013 BQ
3,3 J,AI SURE DE CETTE REPONSE)J'AI TROUVE 4,342*-6
FINALEMET JE M'EXCUSE POUR LES ACCENTS (J'AI PAS LA LANGUE FRANCAISE DANS MA CLAVIER)
Bonjour,
Bienvenue sur le forum et meilleurs voeux !
Remarque : pour écrire des formules, tu as deux outils sur le site (clique sur le raccourci) :
 extrait de
extrait de Q10 - Puis-je insérer des symboles mathématiques afin de faciliter la lecture de mon message ?
1. La désintégration du sodium en magnésium conduit effectivement à une émission
 -
-
Il faudrait cependant que tu écrives l'équation de désintégration !
2. Si le sodium était plus stable que le magnésium, pour quelle raison il se désintègrerait spontanément ?
Lire cette fiche :
3.1. Il faut détailler ton raisonnement !
Vo = 5,00.10-3 L
Co = 1,00.10-3 mol/L
donc no = Co * Vo = 1,00.10-3 * 5,00.10-3 = 5,00.10-6 mol
Je te conseille également d'étudier attentivement cette fiche sur le nombre de chiffres significatifs à donner à ton résultat :
3.2. A justifier !
D'autre part, il manque des données dans ton énoncé : constante de désintégration en particulier.
3.3. Idem, à justifier et donner une unité à ton résultat !
3.4. Que proposes-tu ?

salut, merci de votre reponse .
mes reponse ci-dessus sont en bref car c'est pas mon interet a ce moment c'est pourcela j'ai ecrit just les resultats.
alors pour les donnes ,ui j'ai oblie d'ecrire les donnes 😁
pour l'equation c'est NA====>MG+(-1)e
3.1 c,est ce j'ai fus mais j'ai dis mes repones brievement.(j'ai oblie les double 00 a cote du 5)
3.2 j'ai utiliser la relation suivante a0=lambda *N0. et j'ai remplace lambda par ln2/t1/2 *n0*NA
3,4, j'ai essaye d'utiliser la regle de trois
ona np =====>vp
n1======>vperdu
alors on cherche vperdu
donc vperdu=n1*vp/np =4144,761905 ml

 guide latex
guide latex présent sous la zone de saisie du message. La liste complète des caractères mathématiques est disponible dans le
présent sous la zone de saisie du message. La liste complète des caractères mathématiques est disponible dans le  mode d'emploi du forum
mode d'emploi du forum
