Inscription / Connexion Nouveau Sujet
NO2 et question sur l atome du fer
Bonjour,
Voila j aimerai vous posez 2 questions:
Voila quand j ecrit la molécule de NO2 ,deux structure qui respecte l octet sont possible mais la quelle choisir ? Une doit être plus stable non ? Est c'est celle qui est juste?
Deuxième question :
Quand je fais la configuration électronique du fer j obtient 3d^6 4s2. Je réalise mes cases quantiques et j ai bien 8 e- de valence . Avec 2 DNL et 4 electron libre pouvant réaliser une liaison. Mais pourquoi au lycée avec le modèle k,l,m,n... on disait que le fer passait en fer2+ pour respecter l octet.
Deja l octet n est plus valable a partir de 3eme période car ya la sous-couche d. Alors quelle est le but de l atome de fer de passer en fer2+?
Merci pour l aide
Bonjour
Dans la molécule NO2, le nombre d'électrons de valence est :
5+2x6=17.
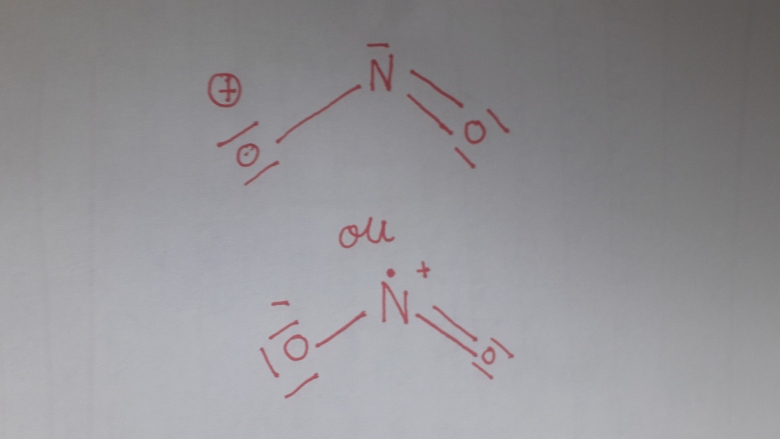
C'est un nombre impair. Il n'est donc pas possible de trouver une formule de Lewis où les trois atomes respectent la règle de L'octect. Cette règle simple est insuffisante pour expliquer toutes les structures moléculaires possibles. Tu verras plus tard la théorie des orbitales moléculaires. Cependant, la mesure de l'angle de liaison : 134° , valeur nettement supérieure à 120°, montre que la structure la plus proche de la réalité est celle faisant apparaître un électrons célibataire sur N. (voir cours sur méthode VSEPR)
Les métaux de transition ont une chimie assez compliquée. Quelques généralités à connaître :
* à l'exception de l'argent, tous les atomes ont tendance à perdre en priorité leurs 2 électrons s ; c'est pour cette raison qu'il forment presque tous des ions 2+ : Fe2+,Cu2+,Zn2+....
* la situation se complique en solution aqueuses car ces ions se stabilisent souvent en s'associant à des molécules d'eau, molécules qu'on ne fait pas figurer dans les équations : on note seulement Cu2+(aq).


