Inscription / Connexion Nouveau Sujet
masse du réactif restant
Bonjour  Alors demain j'ai la semaine blanche et je commence avec physique chimie. Donc je m'entraîne un peu avec les exercices qui sont dans mon livre. Mais problème : il n'y a pas la correction. Donc je me demandais si vous pouviez m'aider, voici le problème :
Alors demain j'ai la semaine blanche et je commence avec physique chimie. Donc je m'entraîne un peu avec les exercices qui sont dans mon livre. Mais problème : il n'y a pas la correction. Donc je me demandais si vous pouviez m'aider, voici le problème :
Énonce :
L'éthanol (de formule C2H6O), liquide incolore et inflammable, brûle dans le dioxygène gazeux. Il se forme alors du dioxyde de carbone gazeux et de l'eau liquide. On fait réagir me,i = 2.50 g d'éthanol et une masse md,i = 2.50 g de dioxygène.
Questions:
a.Ecrire l'équation de la réaction
b.Calculer les quantités de matières initiales d'éthanol et de dioxygène
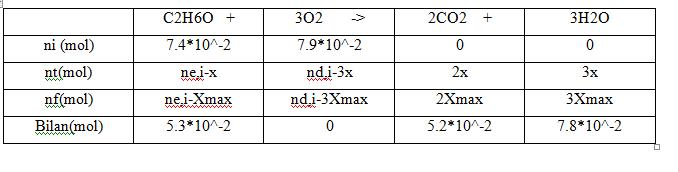
c.Construire le tableau d'évolution
d. Calculer l'avancement Xmax et déterminer le réactif limitant
e.Décrire le système à l'état final
f.Déterminer la masse du réactif restant.
Voilà mes réponses :
a.
C2H6O(l) + O2(g) -> CO2(g) + H2O(l)
<-> C2H6O(l) + 3O2(g) -> 2CO2(g) + 3H2O(l)
b. On sait que n= m/M
Donc :
ne,i = 2.50/(6+2*6+16)
= 7.4*10^-2
nd,i = 2.50/(16*2)
=7.9*10^-2
c.
Si l'éthanol est limitant alors 7.4*10^-2 - x =0
x=7.4*10^-2
Si le dioxygène est limitant alors 7.9*10^-2 - 3x =0
x= 7.9*10^-2/3
= 2.6*10^-2
Donc le dioxygène est le réactif limitant (Voir l'image)
Et la est le problème, à cette question, j'ai tout fais (je n'avais pas lu les autres questions). Alors j'en ai déduis que je ne savais pas ce que "construire un tableau d'évolution" était exactement, cependant, si il est bien fait, ça ne pose pas beaucoup de problème.
Ce que je n'arrive pas à faire c'est déterminer la masse d'un réactif. Pouvez vous m'aidez s'il vous plais ? Merci d'avance