Inscription / Connexion Nouveau Sujet
Le Bleu de Bromothymol BBT
Bonjour tout le monde!
Je viens de commencer un exercice, mais je reste coincer sur la troisième question... Quelqu'un pourrait-il m'aider?
Voici l'énoncé:
Le BBT est un indicateur coloré. C'est une entité qui change de couleur en fonction du pH. A pH <6, le BBT est jaune, à pH=6,8, il est vert et à pH>7,6 il est bleu.
Les courbes spectrales d'une solution de BBT réalisées dans une cuve de 1,0cm à différents pH se trouvent ci-dessous.
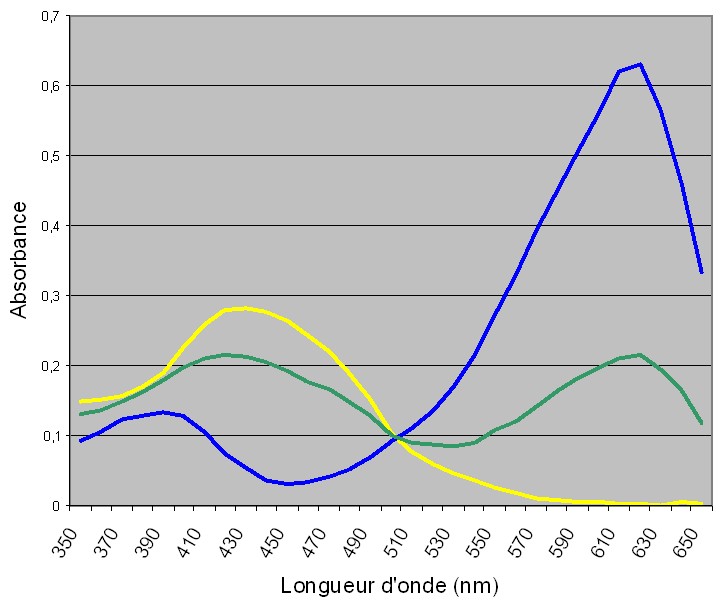
a. Déterminer les longueurs d'onde correspondant aux maxima d'absorption des courbes spectrales tracées pour pH=6,0 et pH=8,0.
Par lecture graphique, j'ai trouvé lambda = 435nm et 595nm.
b. Les longueurs d'onde déterminées précédemment correspondent-elles aux couleurs des solutions de BBT aux pH considérés?
J'ai mis oui, car à l'aide du diagramme des couleurs complémentaires, on peut voir que pour le jaune, c'est le violet, et pour le bleu, c'est le orange. (bien sûr, j'ai plus développé sur ma copie)
c. Sur le spectre tracé pour pH=7,0, il apparait deux pics dont les abscisses correspondent aux longueurs d'onde précédemment trouvées. Proposer une explication.
Voilà, et là je suis perdue ... Selon le a et le b, pour pH=7,0 la solution devrait absorbée du orange et du violet. Or, pour que la solution soit verte (d'après énoncé, pH=6,8 -> Solution verte) , il faut qu'elle absorbe du rouge ...
Quelqu'un pourrait il m'aider? En espérant que je me sois exprimer clairement 
Merci de votre réponse!
Oui c'est vrai qu'avec le graph ce serait plus simple ... le voici! la courbe bleu correspond à pH=8,0, la courbe jaune à pH= 6,0 et la courbe verte, pH=7,0.

 ?
? 
