Inscription / Connexion Nouveau Sujet
La pluie d'or
Voici l'énoncé de l'exercice :
Les ions iodure l-(aq ) et les ions plomb ( II ) Pb2+ ( aq ) réagissent pour former de l'iodure de plomb Pbl2 ( s ). L'équation de la transformation s'écrit : Pb2+ ( aq ) + 2I- ( aq ) = Pbl2 ( s ).
A 25 ° C , la constante d'équilibre est K ( 25 ° C ) = 7,4 x 10^7.
On dissout totalement dans de l'eau distillée une masse m1 : = 5,0 g d'iodure de potassium Kl ( s ) et une masse m2 = 5,0 g de nitrate de plomb Pb( NO3)2 ( s ). Le volume de la solution obtenue est V = 50,0 mL .
1. Calculer le quotient de réaction initial , Quavant toute réaction entre les ions .
n1=m1/M1=5/166=0.030mol
n2=m2/M2=5/331=0.015mol
C(KI)=n1/V=0.030/0.05=0.6mol.L
C(Pb(NO3)=n2/0.05=0.3mol.L
Qr,i= 1/ (0.6)^2 × 0.3 = 9.3
2. Déterminer s'il se forme des cristaux d'iodure de plomb .
Qr,i < K donc pas de cristaux d'iodure de plomb
3. Lorsque le système n'évolue plus : [ [Pb2+ ]= 1.5 x 10 mol.L et [ I- ] = 3,0 x 10 mol.L. Calculer le taux d'avancement final et le quotient de réaction Qr à l'état final A. Conclure .
n1=C(Pb)×V=(1.5×10^-3)×(50×10-3)=7.5×10-5 mol
n2=C(I)×V=(3.0×10-3)×(50×10-3)=1.5×10-4 mol
J'ai fait un tableau d'avancement et j'en ai déduit que Xmax=7.5×10^-5 mol ainsi que ka réaction est totale
Je n'arrive pas a trouvé Xf pour calculer le taux mais je pense que vu que la reaction est total t=1
Qr,a= 1/ (1.5×10^-3)×(3.0×10^-3)=7.4×10^7 Qr,a=K donc il n'y a plus d'évolution
4 .
a ) Le mélange réactionnel décrit en
3. est alors plongé dans un bain - marie thermostaté à 70 ° C ( état B ) . Indiquer la valeur du quotient de réaction Qr,b avant toute nouvelle transformation.
Je n'arrive pas à trouvé comment le changement de température influe sur Qr
b ) La solution devient alors limpide . D'après cette observation , à 70 ° C , comparer Q. la constante d'équilibre K ( 70 ° C ) .
c ) En déduire l'influence de la température sur la constante d'équilibre K de cette réaction .
5. La solution limpide est refroidie dans un bain de glace . Quand la solution change d'aspect , après agitation , une « pluie d'or » apparait . Proposer une explication à la formation des cristaux d'iodure de plomb Pbl ( 8 )
6. La solution est ensuite filtrée . Une pointe de spatule de nitrate de plomb est ajoutée au filtrat . A l'aide du quotient de réaction , discuter du sens d'évolution du système . Données masses molaires en g.mof M ( Pb ( NO ) : 33 ) , M ( KI ) . 166 .
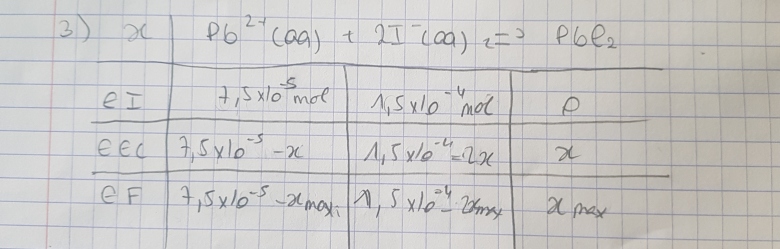
Bonjour
D'accord pour 1 et 2. Pour 3 : la réaction n'est pas totale puisque à l'équilibre :
Qre=K 0
0
Il faut remplir un tableau d'avancement et écrire que l'état final est un état d'équilibre entre les ions restant et le précipité (solide).
Attention : tu n'as pas bien recopié les concentrations des ions à l'équilibre mais le fait que ces concentrations ne soient pas nulles est une autre preuve du fait que la réaction de précipitation n'est pas totale.
Merci de votre réponse. Je ne comprends pas pourquoi la réaction n'est pas totale Qr,A=K celà ne veut pas dire que la reaction est totale?
En effet je me suis trompé lorsque j'ai recopié l'énoncé les concentrations sont 1.5×10^-3 et 3.0×10^-3
J'ai fait un tableau d'avancement il est en bas de mon message, je ne suis pas sûr qu'il soit correcte pour autant.
Qr,i < K donc pas de cristaux d'iodure de plomb
Il n'y a pas de cristaux au départ mais, puisque Qri<K, cet état initial n'est pas un état d'équilibre : il y a donc spontanément réaction dans le sens direct c'est à dire dans le sens de la formation de cristaux. Cette réaction de précipitation conduit à une diminution des concentrations en ions donc à une augmentation de Qr jusqu'à ce qu'un état d'équilibre s'établisse lorsque sera atteinte la condition Qr=K.
C'est ce qu'il faut vérifier puisque sont fournies les concentrations en ions à l'état final d'équilibre.


