Inscription / Connexion Nouveau Sujet
La constante d'équilibre par l'étude condutimétrique (CHIMIE)
Bonjour, j'aimerai avoir vos lumières sur un exercice de chimie, sur l'étude conductimétrique pour déterminez sa constante d'équilibre.
Seul les 3 premières questions je comprends, suite a cela je pourrais faire les autres.
Alors je poste juste les question dont je ne comprend pas 
Enoncé :
On mesure, à 25°C, la conductivité d'une solution d'acide éthanoïque de concentration C2 = 1,0 x 10-1 mol.L-1.
Le conductimètre indique :  = 5,00 x 10-2 S.m-1.
= 5,00 x 10-2 S.m-1.
On rappelle l'équation de la réaction entre l'acide éthanoïque et l'eau :
CH3CO2H(aq) + H2O(l) = CH3CO2-(aq) + H3O+(aq)
1. On néglige toute autre réaction chimique.
Cites les espèces ioniques présentent dans cette solution.
Donner la relation liant leur concentration molaire.
Les espèces ioniques présentent dans cette solution sont, l'ion oxionium H3O+(aq) et l'ion éthanoate CH3CO2-(aq).
Là je ne vois pas quel relation les liant a part que leurs concentration sont égales, soit [H3O+(aq)] = [CH3CO2-(aq)]
2. Donner l'expression littérale de la conductivité  de la solution en fonction des concentrations molaires finales en ions oxonium et en ions éthanoates.
de la solution en fonction des concentrations molaires finales en ions oxonium et en ions éthanoates.
 =
= 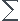

. [X
]
 =
= . [H3O+] +
. [CH3CO2-]
 = [H3O+] . (
= [H3O+] . ( +
)
3. Donner l'expression littérale permettant d'obtenir les concentrations molaires finales des ions en fonction de la conductivité  , et des conductivitées molaires ioniques
, et des conductivitées molaires ioniques et
.
Déterminer la valeur de la concentration molaire finale en ions oxonium et éthanoate en mol.m-3, puis en mol.L-1
Alors là j'ai vraiment rien compris ^^
Merci de bien vouloir m'aider
Groy 
J'ai oublié des données.
Données : condtuctivités molaire ioniques à 25°C :
= 35,9 x 10-3 S.m2.mol-1
= 4,1 x 10-3 S.m2.mol-1
bonsoir , bin pour la question 3) il n'y a plus qu'a utiliser la relation que tu as ecrit dans la question 2 , sauf que l'on cherche [H3O+]



