Inscription / Connexion Nouveau Sujet
La caféine
Bonjour besoin d'aide pour se devoir
La caféine, aussi appelée théine, est un alcaloïde de la famille des méthylxanthines, présent dans de nombreux aliments, qui agit comme stimulant psychotrope et comme léger diurétique. Sa formule chimique est la suivante: 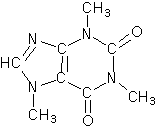
1. Calculer la concentration massique Cm d'une solution de caféine dosée par spectrophotométrie. Dans les conditions du dosage l'absorbance de la solution est A=1,55 et le coefficient d proportionnalité entre A et Cm est ?=3,12×10?2??.??1
2. Déterminer la masse molaire de la caféine.
3. En déduire la concentration molaire de la solution de caféine.
Merci à ceux qui me répondront .
***Image insérée sur le serveur --> merci de faire de même la prochaine fois !***
Bonjour !
1) Tu connais la formule A=k*Cm. Or on te donne A=1,55 et k=...(tu as dus mal l'écrire).
Avec ces 2infos, tu en déduis facilement la concenration, non ?
2)Trouve la formule brute de la caféine a l'aide de la formule développé, et tu calcule la masse molaire.
Alors j'ai trouvé sa pouvez vous me corriger 1) A = 3,12.10⁻² x Cm
A = 1,55
Donc Cm = 1,55/3,12.10⁻² = 49,7 g.mol⁻1
2) La formule brute de la caféine est C₈H₁₀N₄O₂ (on compte tous les atomes sur la formule développée jointe).
On déduit la masse molaire M :
M[C₈H₁₀N₄O₂] = 8x12 + 10x1 + 4x14 + 2x16 = 194 g.mol⁻¹
3) C = Cm/M = 49,7/194 = 0,256 mol.L⁻¹
On retrouve cette formule comme suit :
Cm = m/V
C = n/V
n = m/M ⇒ m = nxM
⇒ Cm = nxM/V = MxC ou C = Cm/M



