Inscription / Connexion Nouveau Sujet
L'electrolyse
Bonjour pouvez vous m'aider sur cette exercice :
Combien de temps faut-il laisser un courant de 1 A dans un voltamètre de sulfate de cuivre former sur la Cathode une couche d'épaisseur uniforme de 0.5mm ? La cathode Est un disque de 2 cm de diamètre et 5 mm d'épaisseur
Masse volumique = 8.9 grammes par centimètre cube
Ici Faut trouver le volume puis la masse puis le temps
Là où je suis bloqué
À partir du volume
Merci d'avance
Oui oui ,voici où est le problème maintenant ,
Je sais qu'on doit le volume de la Cathode avant électrolyse puis après,
Soit V1 et V2
V1 c'est simple on multiplie Pi par le Rayon par l'épaisseur soit V1= pi*r*e1
Il va se former une couche d'épaisseur de 0.5mm à la Cathode
V2 c'est là où j'ai un doute sur l'épaisseur
Ce sera V2 = pi*r*(e1+e2)
Ou V2 = pi*r*e2
?
Bonsoir,
Tout d'abord la formule qui permet de calculer le volume de la cathode " avant " n'est pas comme tu le dis égal à π*r*e1 comme mais à π * r² * e1
Mais je ne pense pas que la méthode que tu exposes soit la meilleure.
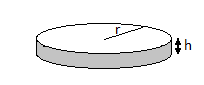
La cathode a la forme d'un cylindre de rayon "r" et de hauteur "h"
La surface de ce cylindre est composée de deux disques de rayon " r " et d'une surface latérale qui sépare ces deux disques.
Chaque disque a une aire égale à π*r²
La surface latérale a une aire de 2*π*r*h
La surface totale S de la cathode est donc S = 2 *π*r² + 2*π*r*h = 2*π*r*(r+h)
Cette surface S est calculable puisque on connaît les valeurs de " r " et de "h "
Une fois S calculée il suffira de la multiplier par l'épaisseur " e " du dépôt de cuivre (connu lui aussi) pour connaître le volume V de ce dépôt.
Finalement V = 2*π*r*(r+h)*e
Je suggère d'utiliser le cm comme unité de longueur.
On obtiendra alors le volume du dépôt de cuivre en cm³ ce qui facilitera le calcul à venir de la masse de ce dépôt.
Quand vous faites allusion à la première épaisseur?
Et puis pourquoi vous affirmez que la Cathode est un cylindre ?
Quand vous faites allusion à la première épaisseur?
Désolé je ne comprends pas cette question.
Et puis pourquoi vous affirmez que la Cathode est un cylindre ?
Je me fie à la description de l'énoncé.
Voir figure
Désolé mais j'echouais en utilisant cette methode , ce qu'il fallait faire V2 = pi* ( e2+r)*(e2+e1)
Puis faire la différenciées V2 et V1
Puis trouver la masse et ainsi de suite
Si j'ai bien compris tes notations " e1 " et " e2 " sont des longueurs.
" r " représente probablement le rayon de la cathode, donc une longueur aussi.
Dans le cadre de ces hypothèses :
(e2 + r) est une longueur.
(e2 + e1) est aussi une longueur.
Alors le produit (e2 + r) * (e2 + e1) qui est le produit de deux longueurs représente une aire.
Et évidemment  *(e2+r)*(e2+e1) représente également une aire et ne peut pas être égal à un volume.
*(e2+r)*(e2+e1) représente également une aire et ne peut pas être égal à un volume.


