Inscription / Connexion Nouveau Sujet
Géométrie des molécules
Bonjour j'ai une activité à faire et je ne comprends pas tout.
Merci d'avance.
2a) pour chaque molécule, examiner la disposition des atomes autour de l'atome central.
2b) comparer les géométrie autour de l'atome central des molécules d'eau et de dioxyde de carbone, d'une part, et celle des molécules d'ammoniaque et de méthanal, d'autres part.
3) choisir un qualificatif pour rencontre de la géométrie autour de l'atome central de chaque molécule.
J'ai mis :
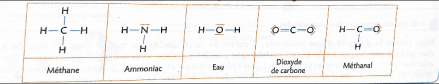
Méthane : tétraédrique
Ammoniac: pyramide à base triangulaire
Eau : coudée
Dioxyde de carbone : linéaire
Méthanal : triangulaire
4) expliquer pourquoi la présence de doublets non liant influence la géométrie autour de l'atome central de chaque molécule.
5) expliquer comment rendre compte de la géométrie autour de l atome central dans une molécule à l'aide de sa représentation de Lewis.
J'ai résolu que la 3, je souhaiterai avoir des pistes pour les autres.
Merci
Cette fiche destinée aux élèves de première pourra sans doute t'aider.
![]() De la structure à l'électronégativité des entités et à la polarité des molécules
De la structure à l'électronégativité des entités et à la polarité des molécules
Donc pour la 2a)
Méthane : atome central C suivi des atomes voisins H qui sont des doublets liants
Ammoniac : atome central C avec les atomes voisins H et une paire non liantes entourants N
Eau : atome central O suivi des atomes voisins H et deux paires non liantes entourants O
Dioxyde de carbone : atome central C suivi des atomes voisins O qui sont des doublets liants et 4 paires non liantes entourants les atomes voisins O
Méthanal : atome central C suivi des atomes voisins H et O et 2 paires non liantes entourants O
La répartition des doublets liants et non liants apparaît dans ton message de 18h27 entre deux carrés noirs.
Pour la 2b) la molécule d'eau et de dioxyde de carbone se ressemble on dirait que la molécule d'eau c'est étendu pour donner la géométrie de la molécule de dioxyde de carbone.
Différence quand même : la molécule CO2 est linéaire (trois noyaux atomiques alignés) alors que la molécule d'eau est coudée à cause de la présence des deux doublets non liants sur l'atome O.
Donc en faisant le même raisonnement
L'ammoniac est une pyramide à base triangulaire avec la présence d'un doublet non liant sur l'azote alors que le methanal est triangulaire dû à la présence de deux paires de doublets non liants sur l'oxygène.
Tu as raison concernant la molécule d'ammoniac : c'est bien la présence du doublet non liant de N qui rend la molécule pyramidale.
Concernant la molécule de méthanal, il faut raisonner sur les liaisons de l'atome C. Il y a trois liaisons(dont une double) et pas de doublet non liant sur C. Les trois axes de liaisons sont dans un même plan, on peut parler de structure triangulaire. Les deux doublets non liants de l'atome O sont conformes à la règle de l'octet mais n'interviennent pas directement dans la géométrie de la molécule.
D'accord merci pour les précisions.
Pour la 4) j'ai pensé à cela comme réponse:
La présence de doubler non liant influencent la géométrie autour de l'atome central de chaque molécule car les doubler d'électrons externes s'écarte au maximum les uns des autres en formant des figures géométriques simples.
D'accord ! Ce sont bien les répulsions entre doublets électroniques d'un même atome qui explique la géométrie de la molécule.