Inscription / Connexion Nouveau Sujet
Exercice sur la synthèse d'une molécule complexe: la phenantoine
Bonjour, mon professeur de physique chimie nous a donné un exercice de niveau et je suis en 1°S. Cet exercice porte sur la synthèse d'une molécule complexe, la phénantoine.
J'ai beaucoup de mal à comprendre cet exercice.
Enoncé: La phénantoine est un médicament utilisé pour traiter l'épilepsie. Cette molécule a été découverte par Justus Liebig en 1838. Il est possible de la synthétiser en deux étapes à partir de la benzoine.
1° étape: synthèse du benzyle
2° étape: synthèse de la phénantoine
Benzyle+urée -> phénantoine+ eau (réaction mole à mole)
Données: M(benzoine)=212g/mol
M(benzyle)=210g/mol
M(phénantoine)=252g/mol
m(urée)=60g/mol
1) La première étape est effectuée à partir de 3g de benzoine et d'un excès d'acétate de cuivre comme oxydant.
a) Calculer la quantité de matière de benzoine introduite.
b) Celle-ci étant introduite en défaut, calculer la masse maximale de benzyle qu'il est possible d'obtenir.
c) Après extraction et purification, une masse m=2.4g de benzyle est obtenue. Calculer le rendement de cette premiere étape.
2) a) Identifier les groupes caractéristiques présents sur la benzoine et le benzyle.
b) Quel groupe est modifié lors de la réaction?
c) conclure: la réaction qui a lieu à cette étape est-elle une oxydation ou une réduction?
d) Est-il possible d'utiliser un test chimique pour déterminer si la réaction a bien eu lieu? Justifier.
3) Le benzyle obtenu (m=2.4g) est chauffé pendant deux heures dans un montage à reflux avec 5g d'urée.
a) Calculer les quantités de matière de benzyle et d'urée mises en jeu et en déduire le réactif limitant.
b) Cette étape s'effectue avec un rendement de 60%: calculer la masse de phénantoine obtenue.
4) Quel est le rendement global de cette synthèse?
A la question 1 a, j'ai trouvé une quantite de matière égale à 0.014 mol!
Merci beaucoup de vos réponses que j'attend avec impatience.
bonjour,
Il ne faut pas se laisser impressionner par les formules inhabituellement compliquées pour la 1ère S.Toutes les questions peuvent être résolues avec un niveau 1S
Je suppose qu'on t'a fourni les équations de réactions.(j'écrirais plutôt benzile que benzyle)sinon une recherche avec google y remédiera!
1a) OK
b) on te dit que le réactif limitant est la benzoïne .
d'autre part , une mol de benzoïne oxydée donne 1 mol de benzile.
Quelle est donc la qté max de benzile que l'on peut obtenir?
Puis calculer la masse.
c) rendement 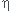
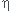 =( masse obtenue expérimentalement/masse maximale théorique)*100
=( masse obtenue expérimentalement/masse maximale théorique)*100
2)a)il y en a 2 que tu dois connaître
b) il suffit de regarder les formules
c) 2 façons de répondre
relire le 1)a
utiliser la réponse 2)b et des résultats de cours ou TP
d)le benzoïle contient une fonction que tu as appris à reconnaître expérimentalement (enfin je suppose !)
je te laisse réfléchir pour trouver la réponse à la question.
3) on te dit que la réaction se fait mol à mol ,c'est à dire que
1 mol d'urée réagit avec 1 mol de benzile pour donner 1 mol de phénantoïne + eau
4) le rendement global est le produit des 2 rendements


