Inscription / Connexion Nouveau Sujet
Exercice sur l'hydrogène
Bonjour,
Je suis en première ES et j'ai un devoir sur la séquence du défi énergétique que je trouve assez compliqué... Pouvez-vous m'aider à le comprendre svp ?
J'ai mis en italique ce que j'ai répondu, pouvez vous me dire si c'est correct, sinon m'expliquer mes erreurs ?
Exercice :
(Il faut répondre aux questions après chaque paragraphe correspondant)
La combustion de l'essence dans l'air fournit de l'énergie. Mais cette combustion provoque un dégagement de dioxyde de carbone qui est un gaz à effet de serre.
La réaction du dihydrogène (H2) avec le dioxygène (O2) fournit aussi de l'énergie, mais cette combustion ne donne pas de dioxyde de carbone.
Question 1 :
a) Qu'appelle-t-on gaz à effet de serre ? Les gaz à effet de serre sont des gaz néfastes pour l'atmosphère à trop grande quantité. Ils sont à l'origine du réchauffement climatique
b) Quel produit de réaction fournit la combustion du dihydrogène dans le dioxygène ? Écrire l'équation de cette réaction. De l'eau est fournit par cette combustion. L'équation : 2H2 + 02 → H20
Cette réaction peut être réalisée en faisant brûler directement le dihydrogène dans le dioxygène, l'énergie est alors libérée par la réaction sous forme de chaleur. Mais on peut également faire réagir le dihydrogène avec le dioxygène dans une pile à combustible. Il y a alors passage du courant dans le circuit d'utilisation connecté aux deux électrodes et une partie de l'énergie dégagée par la réaction chimique est transformée en énergie électrique. Le dioxygène étant abondant dans l'air, on dispose ainsi, avec un réservoir de dihydrogène, d'une source d'énergie propre.
Question 2 :
a) On a représenté ci-contre le schéma de fonctionnement d'une pile à combustible. On indique ci-dessous les réactions qui se produisent à l'anode et à la cathode d'une telle pile :
Réaction à l'anode : H2 → 2H+ + 2e-
Réaction à la cathode : O2 + 4H+ + 4e- → 2H20
En déduire les polarités de la pile. Je ne sais pas ce que sont les polarités...
b) Dans les réactions écrites ci-dessus, deux électrons sont libérés à l'anode alors que quatre électrons sont captés à la cathode. Que répondriez vous à quelqu'un qui vous demanderait d'où viennent les deux électrons en trop ?
Malheureusement, le dihydrogène n'existe pas à l'état naturel. On peut le fabriquer à partir de l'eau liquide, mais il faut bien reconnaître alors que l'utilisation de dihydrogène «source d'énergie propre» revient bien souvent à déplacer le problème de la pollution sans le supprimer.
Question 3 :
a) Indiquer comment on produit industriellement du dihydrogène à partir de l'eau liquide. On peut produire du dihydrogène avec des hydrocarbures ou des électrolytes.
b) Expliquer pourquoi on peut dire bien souvent qu'on a simplement déplacé le problème de la pollution sans le supprimer quand on utilise du dihydrogène comme source d'énergie propre. Car il faut produire l'hydrogène.
La meilleure solution est d'utiliser des panneaux solaires photovoltaïques placés sur le toit des habitations. L'énergie solaire est alors transformée en énergie électrique, ce qui permet de décomposer l'eau en dihydrogène et dioxygène. Le dihydrogène doit ensuite être stocké pour permettre de faire fonctionner les appareils électroménagers même lorsque
l'ensoleillement a disparu. Le dihydrogène obtenu peut également être utilisé pour faire fonctionner des véhicules. Mais ce stockage du dihydrogène pose problème puisque il est
gazeux à température ambiante et ne se liquéfie qu'à - 253°C. Toutefois, il peut être stocké sous forme de composés métalliques solides appelés hydrures. Pour assurer les besoins
d'une famille européenne (hors chauffage) pendant une semaine, il faudrait stocker trois ou quatre kilogrammes de dihydrogène.
Question 4 :
a) Pourquoi le stockage d'un gaz est-il plus problématique que celui d'un liquide comme l'essence ? Car il ne se liquéfie qu'à -253°C.
b) Sachant que la combustion d'un kilogramme de dihydrogène libère une énergie de 120 MJ dont environ la moitié peut être convertie en électricité dans une pile à combustible, quelle masse de dihydrogène faut-il stocker pour assurer une semaine de consommation pour une famille française si on admet que l'énergie dépensée (hors chauffage) vaut en moyenne 3000 kilowattheures par an ?
Voilà j'ai vraiment besoin d'aide, merci 
Salut,
a) Qu'appelle-t-on gaz à effet de serre ? Les gaz à effet de serre sont des gaz néfastes pour l'atmosphère à trop grande quantité. Ils sont à l'origine du réchauffement climatique
--> en quoi sont-ils néfastes ? En quoi sont-ils à l'origine du réchauffement climatique ?
b) Quel produit de réaction fournit la combustion du dihydrogène dans le dioxygène ? Écrire l'équation de cette réaction. De l'eau est fournit par cette combustion. L'équation : 2H2 + 02 → H20
--> ton équation n'est pas équilibrée ...
Question 2 :
a) On a représenté ci-contre le schéma de fonctionnement d'une pile à combustible. On indique ci-dessous les réactions qui se produisent à l'anode et à la cathode d'une telle pile :
Réaction à l'anode : H2 → 2H+ + 2e-
--> OUI ! TB !
Réaction à la cathode : O2 + 4H+ + 4e- → 2H20
--> OUI ! TB !
En déduire les polarités de la pile. Je ne sais pas ce que sont les polarités...
--> on te demande de dire quel est le pole "+" et le pole "-".
Pour rappel, dans un circuit électrique, les électrons se déplacent dans quel sens ?
Quelle est la conséquence sur la polarité ?
b) Dans les réactions écrites ci-dessus, deux électrons sont libérés à l'anode alors que quatre électrons sont captés à la cathode. Que répondriez vous à quelqu'un qui vous demanderait d'où viennent les deux électrons en trop ?
A ton avis ?
Malheureusement, le dihydrogène n'existe pas à l'état naturel. On peut le fabriquer à partir de l'eau liquide, mais il faut bien reconnaître alors que l'utilisation de dihydrogène «source d'énergie propre» revient bien souvent à déplacer le problème de la pollution sans le supprimer.
Question 3 :
a) Indiquer comment on produit industriellement du dihydrogène à partir de l'eau liquide. On peut produire du dihydrogène avec des hydrocarbures ou des électrolytes.
--> Oui, un lien pour plus d'infos
A partir d'une électrolyse de l'eau, pour être plus précis.
b) Expliquer pourquoi on peut dire bien souvent qu'on a simplement déplacé le problème de la pollution sans le supprimer quand on utilise du dihydrogène comme source d'énergie propre. Car il faut produire l'hydrogène.
Si on fabrique du dihydrogène :
--> à partir d'hydrocarbure : on libère du CO2 lors de la réaction ... Donc, même si c'est plus rentable actuellement, tu aurais des voitures roulant à l'hydrogène, donc propres ... mais dont la production libèrerait du CO2 => intérêt nul ...
--> à partir d'une électrolyse de l'eau : là aussi il faut faire attention.
En effet, actuellement dans le monde, autour de 60% de l'électricité est produite à partir d'énergies fossiles ! Donc de la même façon, tu aurait de l'hydrogène fabriqué de façon propre, des voitures roulant de façon propre, mais une électricité produite de façon "sale" => tout dépend donc du mode de production nécessaire à l'électrolyse.
La meilleure solution est d'utiliser des panneaux solaires photovoltaïques placés sur le toit des habitations. L'énergie solaire est alors transformée en énergie électrique, ce qui permet de décomposer l'eau en dihydrogène et dioxygène. Le dihydrogène doit ensuite être stocké pour permettre de faire fonctionner les appareils électroménagers même lorsque l'ensoleillement a disparu. Le dihydrogène obtenu peut également être utilisé pour faire fonctionner des véhicules. Mais ce stockage du dihydrogène pose problème puisque il est
gazeux à température ambiante et ne se liquéfie qu'à - 253°C. Toutefois, il peut être stocké sous forme de composés métalliques solides appelés hydrures. Pour assurer les besoins d'une famille européenne (hors chauffage) pendant une semaine, il faudrait stocker trois ou quatre kilogrammes de dihydrogène.
Question 4 :
a) Pourquoi le stockage d'un gaz est-il plus problématique que celui d'un liquide comme l'essence ? Car il ne se liquéfie qu'à -253°C.
--> donc pour pouvoir le liquéfier, deux solutions :
soit réduire sa température jusqu'à -253°C en conditions de pression normales => demande de l'énergie
soit le comprimer pour également le liquéfier
b) Sachant que la combustion d'un kilogramme de dihydrogène libère une énergie de 120 MJ dont environ la moitié peut être convertie en électricité dans une pile à combustible, quelle masse de dihydrogène faut-il stocker pour assurer une semaine de consommation pour une famille française si on admet que l'énergie dépensée (hors chauffage) vaut en moyenne 3000 kilowattheures par an ?
--> que proposes-tu ?

Merci d'avoir pris du temps pour me répondre !
Alors,
Q1 a) Ils sont néfastes car ils font des trous dans la couche d'ozone ? Ce qui laisse passer plus de chaleur et donc réchauffe notre planète ?
b) Oui j'avais mal recopié : 2H2 + 02 → 2H20
Q2 a) les équations font parti de l'ennoncé  je n'aurais pas pu trouver ça je pense
je n'aurais pas pu trouver ça je pense  Le courant se déplace de la borne positive à négative ? (En réalité je ne sais plus vraiment car au collège on m'avait dit qu'il y avait un sens réel et un sens conventionnel...) La borne positive est anode et la négative est la cathode ?
Le courant se déplace de la borne positive à négative ? (En réalité je ne sais plus vraiment car au collège on m'avait dit qu'il y avait un sens réel et un sens conventionnel...) La borne positive est anode et la négative est la cathode ?
b) Les électrons en trop viennent de la transformation ?
Q3 a) et b) Merci pour l'info, dans mon cours ça n'est pas dit donc j'en apprends plus 
Q4 a) Donc je dois dire que le stockage d'un gaz est plus problématique que celui d'un liquide car la liquéfaction ne se fait qu'à -253°C ce qui demande de l'énergie et/ou une compression ?
b) J'ai vu sur un autre forum ce raisonnement :
3000 kilowattheures par an
52 semaines par an
3000 / 52 = 57.7
Ensuite il faut convertir les kWh en MJ sachant que 1 kWh = 3,6 MJ
57.7 x 3.6 = 207.72 MJ
1kg de dihydrogène donne 120MJ
207.72/120 = 1.731
Il faut donc stocker 1.731 Kg de dihydrogène
Je le comprends à moitié ; je ne vois pas pourquoi on utilise le nombre de semaines que contient une année. Car c'est un devoir que je devrai faire sans outils et une personne ne connait pas forcément le nombre de semaines qu'il y a dans une année.. (ou alors je suis bête!). Ensuite je ne vois pas quelle pourrait être l'unité de 57.7. Mais pour finir je comprends la réponse. Ah et j'oubliais, dans le texte on nous donne les chiffres "trois ou quatre kg de H2". Faut-il les prendre en compte ?
Encore merci !
Petite rectification pour la dernière question :
J'ai en fait compris le raisonnement! 57.7 c'est la consommation hebdomadaire en kWh et donc on veut la convertir en MJ ! Pour le reste (nombre de semaines et données en plus) je ne sais toujours pas mais ça n'empêche pas à la compréhension 
Alors,
Merci d'avoir pris du temps pour me répondre !
Alors,
Q1 a) Ils sont néfastes car ils font des trous dans la couche d'ozone ? Ce qui laisse passer plus de chaleur et donc réchauffe notre planète ?
--> Attention c'est faux ! Ce ne sont pas les gaz à effet de serre qui détruisent la couche d'ozone !
C'est un composé qui était présent dans les aérosols notamment.
Je te conseille de jeter un coup d'oeil ici :http://www.futura-sciences.com/magazines/environnement/infos/dico/d/climatologie-effet-serre-966/
b) Oui j'avais mal recopié : 2H2 + 02 → 2H20
-->

Q2 a) les équations font partie de l'énoncé je n'aurais pas pu trouver ça je pense Le courant se déplace de la borne positive à négative ? (En réalité je ne sais plus vraiment car au collège on m'avait dit qu'il y avait un sens réel et un sens conventionnel...) La borne positive est anode et la négative est la cathode ?
Un rappel du cours d'électricité :
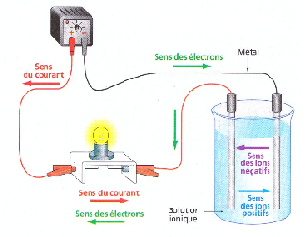
donc dans ta pile :
Réaction à l'anode : H2 → 2H+ + 2e- => elle libère des électrons qui vont du pole négatif au pole positif (sens contraire du courant)
=> ils partent donc du pole "-" = ANODE dans une pile
Réaction à la cathode : O2 + 4H+ + 4e- → 2H20 => point d'arrivée des électrons = pole "+"
b) Les électrons en trop viennent de la transformation ?
=> pourquoi ?
(H2 → 2H+ + 2e-) x2
O2 + 4H+ + 4e- → 2H20
_________________________________
2H2 + O2 --> 2H2O
Q3 a) et b) Merci pour l'info, dans mon cours ça n'est pas dit donc j'en apprends plus
--> Il faut être curieux sur les enjeux de transition énergétique, c'est d'actualité en plus

Q4 a) Donc je dois dire que le stockage d'un gaz est plus problématique que celui d'un liquide car la liquéfaction ne se fait qu'à -253°C ce qui demande de l'énergie et/ou une compression ?
--> Pour une même quantité, un gaz nécessite plus de volume qu'un liquide, donc sous forme gazeuse, il ne serait pas envisageable de le stocker dans des réservoirs de taille acceptable, il faut donc mieux le stocker sous forme de liquide
b) J'ai vu sur un autre forum ce raisonnement :
Citation :
3000 kilowattheures par an
52 semaines par an
3000 / 52 = 57.7 --> unité ? C'est ce qui est consommé en énergie par semaine oui.
Ensuite il faut convertir les kWh en MJ sachant que 1 kWh = 3,6 MJ
57.7 x 3.6 = 207.72 MJ --> OUI !
1kg de dihydrogène donne 120MJ --> d'après l'énoncé
207.72/120 = 1.731
Il faut donc stocker 1.731 Kg de dihydrogène --> OUI !
Je le comprends à moitié ; je ne vois pas pourquoi on utilise le nombre de semaines que contient une année. Car c'est un devoir que je devrai faire sans outils et une personne ne connait pas forcément le nombre de semaines qu'il y a dans une année.. (ou alors je suis bête!).
--> alors là, un examinateur te flingue si tu ne connais pas le nombre de semaines dans une année
 !
!
Ensuite je ne vois pas quelle pourrait être l'unité de 57.7. --> Bah le kWh puisque la consommation annuelle est de 3000 kWh !
Mais pour finir je comprends la réponse. Ah et j'oubliais, dans le texte on nous donne les chiffres "trois ou quatre kg de H2". Faut-il les prendre en compte ?
--> d'après l'énoncé :
Pour assurer les besoins d'une famille européenne (hors chauffage) pendant une semaine, il faudrait stocker trois ou quatre kilogrammes de dihydrogène.
donc les 1,731 kg c'est la consommation hypothétique d'H2 HORS CHAUFFAGE.
Tu comprends mieux pourquoi actuellement la consommation d'énergie explose en hiver ...
Merci beaucoup pour votre aide  C'est bien mieux et bien plus intéressant de comprendre un exercice !
C'est bien mieux et bien plus intéressant de comprendre un exercice !


