Inscription / Connexion Nouveau Sujet
Accueil l'île de la physique - chimie Forum de physique - chimieListe de tous les forums de physique - chimie LycéeOn parle exclusivement de physique/chimie, niveau lycée. TerminaleForum de terminale ChimieTopics traitant de Chimie [tout]Lister tous les topics de physique - chimie
gbm @ 02-02-2015 à 11:48
Cf. le topic posté le 01-02-15 à 20:14
Cf. le topic posté le 01-02-15 à 20:14
Citation :
à 20°C le volume molaire vaut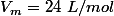
 = \dfrac{V(H_2)}{V_m}=\dfrac{0,1}{24}=...~ mol)
Comme je t'ai expliqué, cette deuxième question est indépendante de la première.
De ce fait, tu ne peux pas utiliser la question 1 car on était dans des proportions stoechiométriques et on cherchait la quantité de dihydrogène nécessaire.
Ici ce n'est plus le cas, on reprend juste la quantité de matière initiale d'oxyde de fer calculée :
 = \dfrac{m_i(Fe_2O_3)}{M(Fe_2O_3)}= \dfrac{5,742}{2 \times 56 + 3 \times 16}= 0,0359 ~mol)
et
 = \dfrac{V(H_2)}{V_m}=\dfrac{0,1}{24}=...~ mol)
Il faut alors déterminer qui est le réactif limitant.
Tu peux t'aider d'un tableau d'avancement.
à 20°C le volume molaire vaut
Comme je t'ai expliqué, cette deuxième question est indépendante de la première.
De ce fait, tu ne peux pas utiliser la question 1 car on était dans des proportions stoechiométriques et on cherchait la quantité de dihydrogène nécessaire.
Ici ce n'est plus le cas, on reprend juste la quantité de matière initiale d'oxyde de fer calculée :
et
Il faut alors déterminer qui est le réactif limitant.
Tu peux t'aider d'un tableau d'avancement.
Je ne comprends pas pourquoi vous avez cité pour 20°c le volume massique est de 24 car ce n'est écrit nul par dans l'énoncé ?


