Inscription / Connexion Nouveau Sujet
Tu dis avoir trouvé 10,3 mL pour Véq mais à la question 3) nous avons dit que 0,100Véq=1/971 avec 0,100 en mol/L et Véq en L. Soit 100Véq=1/971 avec 100mol/mètres cubes et Véq en mètres cubes. Véq=1/(971*100)=1,03.10-5m3=1,03.10-5.103dm3=1,03.10-2dm3=1,03.10-2L=1,03.10-2.103mL=10,3mL
Tu peux aussi faire avec 0,100 mol/L :
0,100 Veq = 1/971
Veq = 10,298661.10-3 L
Veq = 10,3 mL (puisqu'il y a 3 chiffres significatifs)
Comme c'est une droite, il suffit de calculer pour :
V(mL) 0 10 10,1 10,2 10,3
Je te mets le détail du calcul
Pour la 2ème :
 =
=  OH- [OH-] +
OH- [OH-] +  Na+ [Na+] +
Na+ [Na+] +  NH2SO3- [NH2SO3-]
NH2SO3- [NH2SO3-]
en mol.m-3
en mol.m-3
en mol.m-3
Si Veq = 10,3 mL
Avec V en mL :
Avec l'approximation V + V1 + Veau  V1 + Veau = 200 mL
V1 + Veau = 200 mL
Non, le dénominateur reste en m3 parce que V n'y figure pas.
Au numérateur, il ne s'agit que d'un jeu d'écriture. Je remplace Vm3 par VmL.10-6.
C'est plus pratique pour faire le calcul mais VmL.10-6, c'est en m3, en fait.
A partir de V = 10,3 mL, tu utilises la 2ème formule.
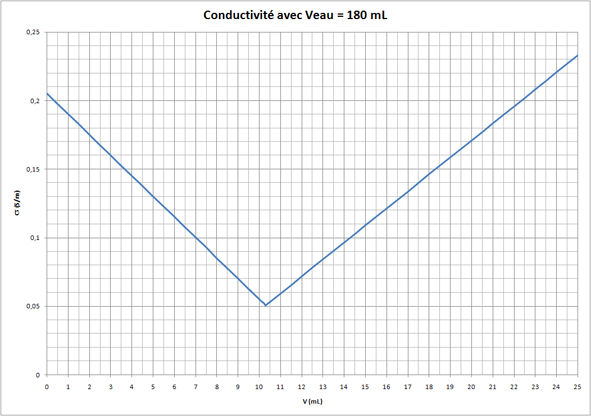
C'est aussi une droite (à cause de l'approximation) et tu peux faire le calcul pour :
V(mL) 10,3 10,5 11 25
C'est suffisant
Et pour la première formule, je ne dois pas prendre 10,3mL comme valeur? lesquelles prendre?
De plus, sur mon graphique V doit être en mL et dans les formules il est en m3... C'est un détail mais je ne comprends pas ce jeu d'unités
Et pour la première formule, je ne dois pas prendre 10,3mL comme valeur? lesquelles prendre?
Tu fais le calcul de 0 à 10,3 mL. Avec les valeurs que j'ai indiquées précédemment, c'est suffisant...
De plus, sur mon graphique V doit être en mL et dans les formules il est en m3... C'est un détail mais je ne comprends pas ce jeu d'unités
Si tu prends les formules sur la dernière ligne dans les deux messages où le calcul est développé, V est en mL (comme c'est indiqué).
Mais si ça te gêne, fais le calcul en m3... C'est moins pratique, c'est tout...
C'est basé sur le fait que, par exemple, 5 mL peut s'écrire 5.10-6 m3.
Donc le 5, c'est des mL en fait mais, dans la formule, il est en m3 parce qu'on a écrit 5.10-6.
Je ne sais pas si c'est plus clair...
Si on remplace V par 10,3mL avec la première formule puis l'autre on trouve le même point de toute façon non?
Si je remplace V par 3mL dans la première formule qui est  =(-3,00.10-6*V+41.10-6)/(0,2.10-3) alors je trouve
=(-3,00.10-6*V+41.10-6)/(0,2.10-3) alors je trouve  =0,16 S.m-1 C'est juste?
=0,16 S.m-1 C'est juste?
J'ai pris comme échelle en ordonnées 3cm correspond à 0,05 donc sur le graphique je place le point à 9,6cm de l'ordonnée à l'origine .
Si tu regardes sur mon graphique, tu verras que c'est bon. Pour V = 3 mL, on trouve  = 0,16 S.m-1 effectivement.
= 0,16 S.m-1 effectivement.
J'ai pris comme échelle en ordonnées 3cm correspond à 0,05 donc sur le graphique je place le point à 9,6cm de l'ordonnée à l'origine .
Ton graphique va faire environ 15 cm de haut. Oui, ça fait 9,6 cm.
Essaye 2,5 cm pour 0,05, je pense que c'est mieux.
Je dois m'absenter un peu.
Bon je réfléchis aux questions 5b), 6) et 7) 
Je serai là ce soir et demain aussi.
Prend ton temps !
Je te remercie encore, tout est très bien expliqué 
5b)On a les deux expressions:
1ère
 =-3,00.10-6V+41.10-6/(V+V1)
=-3,00.10-6V+41.10-6/(V+V1)
2ème
 =2,481.10-6V-15,42.10-6/(V+V1)
=2,481.10-6V-15,42.10-6/(V+V1)
Or V1= 20,0mL= 20,0.10-6 m3
Dans ces expressions faut il remplacer V1 par 20,0 ou 20,0.10-6 ? et pourquoi?
On remplacera donc V à deux endroits dans chaque expression..
On fait toujours la différenciation à V=10,3mL?

Il faut remplacer V1 par 20,0.10-6 parce que V1 doit être en m3.
Je rappelle que les volumes doivent être en m3 parce que les conductivités molaires  sont S.m2.mol-1 (ou mS.m2.mol-1). Il faudrait mettre les conductivités molaires
sont S.m2.mol-1 (ou mS.m2.mol-1). Il faudrait mettre les conductivités molaires  en S.cm2.mol-1 pour utiliser les mL directement (1 mL = 1cm3) mais on aurait
en S.cm2.mol-1 pour utiliser les mL directement (1 mL = 1cm3) mais on aurait  en S.cm-1
en S.cm-1  .
.
V doit être remplacé par la valeur de V (entre 0 et 25 mL) mais V doit être en m3.
On peut évidemment écrire comme précédemment Vm3 = VmL.10-6.
Au dénominateur, là, on ne peut pas négliger V parce que l'on a V + V1. V est du même ordre de grandeur que V1 ( V1 = 20,0 mL et 0 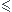 V
V 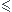 25 mL).
25 mL).
On a V au numérateur et au dénominateur donc nous n'avons plus des droites.
Et l'expression de  change toujours à Veq = 10,3 mL puisque l'expression 0,100 Veq = 1/971 est toujours valable.
change toujours à Veq = 10,3 mL puisque l'expression 0,100 Veq = 1/971 est toujours valable.
Finalement on a :
 =(-3,00.10-6V+41.10-6/(V+20,0.10-6)
=(-3,00.10-6V+41.10-6/(V+20,0.10-6)
et
 =(2,481.10-6V-15,42.10-6/(V+20,0.10-6)
=(2,481.10-6V-15,42.10-6/(V+20,0.10-6)
On peut alors remplacer V par les différentes valeurs, mais faut il changer de formule à V=10,3mL comme pour l'autre graphique?
Je voudrais te demander ton avis sur un message que j'ai reçu sur un autre topic, message qui m'a laissé perplexe...
Si tu veux aller voir, je te donnerai l'adresse où se trouve le message en question...
Je ne voudrais pas faire une mauvaise interprétation.
On peut alors remplacer V par les différentes valeurs, mais faut il changer de formule à V=10,3mL comme pour l'autre graphique?
Exactement

Je ne suis pas sûre de pouvoir t'aider mais je veux bien essayer..
Sinon, les expressions de mon dernier message sont elles justes? Je peux remplacer V?

https://www.ilemaths.net/forum-sujet-321984.html#msg2764161
Message "Posté le 11-12-09 à 20:30"
Tu es libre de me donner ton avis ou pas, bien sûr...
Je suis vraiment désolée mais le temps que je comprenne l'énoncé, le raisonnement de l'élève ,où est le problème et comment le résoudre.... ça mettrait du temps, en plus je ne veux pas dire de bêtises. Demande plutôt à un "modérateur" (je ne sais pas si c'est le bon terme, correcteur officiel?) qui sera plus à même de t'aider 
Restes tu tout de même sur mon topic? Je compte le boucler 
Bien sûr, je reste sur ton topic, ça n'a rien à voir...
Mais je ne te demande de comprendre l'énoncé ni quoi que ce soit de ce genre. Je n'ai pas de problème avec l'énoncé mais avec le contenu du message cité. La question est pourquoi ce message ? C'est quand même surprenant, non ?
Je n'avais pas vu qu'il s'agissait du message de 20h30.. Hum c'est vrai que c'est bizarre, peut être t'a t il senti occupé? En plus ce que tu écris dans ce topic est juste..
Je voulais m'assurer qu'il ne s'agissait pas d'une mauvaise interprétation de ma part.
Bon, laissons tomber...
Continuons la chimie
Sorry, je ne t'ai pas fais avancé beaucoup ..
Pour la première formule qui est  =-3,00.10-6+41.10-6/(V+20,0.10-6)
=-3,00.10-6+41.10-6/(V+20,0.10-6)
Si je remplace V par 3mL je trouve  =1,06.10-5S.m-1, ça me parait faux
=1,06.10-5S.m-1, ça me parait faux
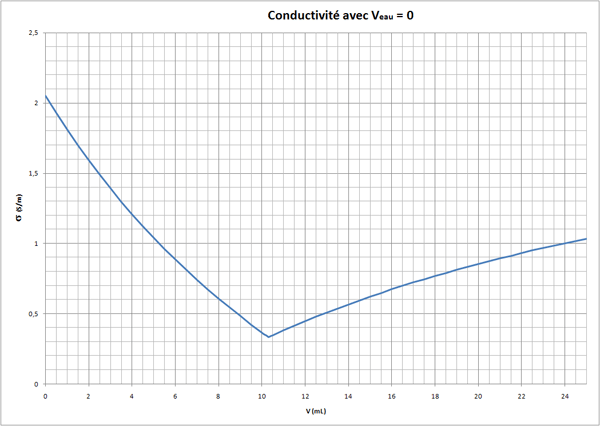
Je trouve pour la première formule:
pour V=0mL, sigma=2,05 S/m, V=3mL sigma=1,4 S/m, pour V=6mL sigma=0,8S/m, pour V=9mL sigma=0,5 S/m pour V=10,3 sigma=0,3 S/m
Je relie les points à la main? ça me fait une courbe "en creux"
Pour V = 6 mL, c'est plutôt 0,9 S/m ( 0,885 )
Pour V = 9 mL, je trouve 0,484 S/m. Donc 0,5 est acceptable (pas très précis).
Il faut relier les points.
Cela donne une courbe comme celle du message précédent.
Oui je vais prendre des valeurs plus précises, je trouve les même que toi  Je finis de tracer et je passe à la suite !
Je finis de tracer et je passe à la suite !
6) Comment démontrer que pour les deux graphiques l'abscisse du point singulier est V=Véq? Je ne comprends pas la question
Oui, ce n'est pas clair comme question...
Je pense à ce genre de réponse.
La conductivité molaire de NH2SO3- est égale à 4,83 mS.m2.mol-1.
La conductivité molaire de Na+ est égale à 5,01 mS.m2.mol-1.
Donc environ 5 mS.m2.mol-1 pour les deux.
La conductivité molaire de H3O+ est égale à 35,0 mS.m2.mol-1 soit environ 7 fois plus que NH2SO3- et Na+.
Donc la conductivité globale, pour la première partie, est essentiellement due à H3O+.
Si la concentration de H3O+ diminue, la conductivité diminue. Quand elle est nulle, la conductivité est la plus faible.
La conductivité molaire de OH- est égale à 19,8 mS.m2.mol-1 soit environ 4 fois plus que NH2SO3- et Na+.
Donc la conductivité globale, pour la deuxième partie, est essentiellement due à OH-.
Quand la conductivité augmente, c'est lorsque la concentration en OH- augmente.
Donc le point qui correspond à la conductivité la plus faible correspond bien à V = Veq, volume pour avoir [H3O+] = [OH-] = 0.
Le "point singulier" dont il est question, est, bien sûr, le "point de cassure" sur les courbes.
Mais la question est bizarre puisque les courbes ont été faites en utilisant Veq comme limite des deux parties de la courbe.
A demain
A V = Veq, on a bien les concentrations en H3O+ et OH- qui sont nulles.
A V = Veq, il n'y a plus de H3O+ (tous "consommés") et pas encore de OH-.