Inscription / Connexion Nouveau Sujet
Étude du cuivre et de sa protection
Bonjour, j'ai un dm de chimie auquel je n'arrive guère, j'espère que vous pourrez m aider. Merci d'avance.
La trompette est basée sur le cuivre.
Il s'oxyde facilement au contact du dioxygène de l'air et de l'eau. Afin de le proteger, les artisans luthiers doivent procéder à une électrolyse. Cette technique nécessite un générateur, des câbles électriques, une électrode de graphite, des minces en platine et une bassine de solution aqueuse acide d'ion argent et nitrate dans laquelle plongent la trompette et le graphite. La trompette, l'électrode de graphite, le générateur et la solution aqueuse constituent un circuit en série. La bassine présente un dégagement de bulles de gaz sur l'électrode de graphite. Apres un certain temps delta T, l'instrument de cuivre ressort totalement couleur argent. L'aspect et le toucher de l'argenture sont sans aspérités, lisses et homogènes.
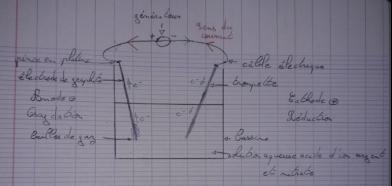
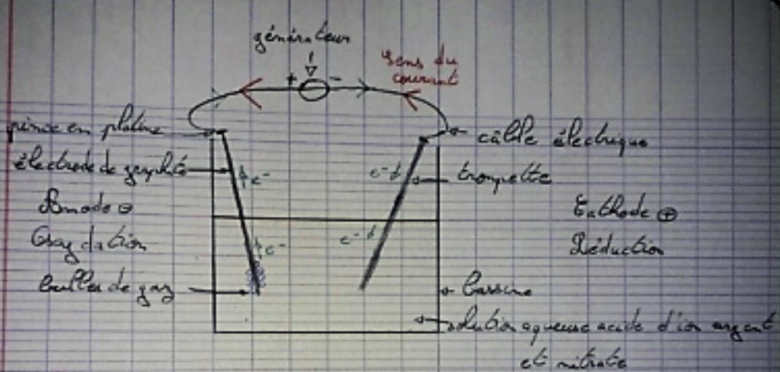
1) Proposer un schéma du montage expérimental avec le matériel donné.
2) quelle propriété de la trompette utilise t on vis à vis du courant électrique ?
3) quelle réaction subissent les ions argent ?
4) en conséquence, quel nom porte les électrodes de graphite et l'instrument de musique ?
5) de quelle manière, au sein de la matière, se déplacent les électrons dans la trompette et l'électrode de graphite ?
6) compléter le schéma avec le sens du courant, le sens de déplacement des électrons et une illustration sommaire de ce qui se passe aux électrodes.
7) donner la demi équation électronique du second couple redox mis en jeu.
8) que représentent les ions nitrates vis à vis de la réaction ?
9) donner l'équation de réaction mise en jeu alors.
10) en utilisant un tableau d'avancement, établir la relation entre la quantité de matière de l'argent et celle du gaz produits.
Bonjour,
En vertu de ceci :
Je te conseille de commencer par étudier attentivement cette fiche (et celle sur la pile) :
Une fois que ce sera fait, tu pourras me proposer tes piste de réflexion pour qu'on échange là-dessus
Bonjour,
désolé, évidemment je ne voulais pas vous laisser faire le travail à ma place.
Donc en partant de la seconde question donc, je pense que la propriété de la trompette que l'on utilise vis à vis du circuit électrique est le métal sur lequel il est basé, donc le cuivre ?
Pour la question 3, la réaction que subissent les ions argent est un réduction ? Pour la question 4, l'électrode de graphite est la cathode et le cuivre l'anode ?
Pour la question 3, la réaction que subissent les ions argent est un réduction ? Pour la question 4, l'électrode de graphite est la cathode et la trompette l'anode ?
Il me semble avoir réussi la première question mais à partir de la seconde je n'y arrive pas.
Peux-tu poster le schéma que tu as fait ?
 extrait de
extrait de Q05 - Puis-je insérer une image dans mon message ? Comment faire ? Quelle image est autorisée ?
Donc en partant de la seconde question donc, je pense que la propriété de la trompette que l'on utilise vis à vis du circuit électrique est le métal sur lequel il est basé, donc le cuivre ?
Cela ne répond pas à la question : quelle est la propriété électrique d'un métal comme le cuivre ?
Pour la question 3, la réaction que subissent les ions argent est un réduction ? Pour la question 4, l'électrode de graphite est la cathode et le cuivre l'anode ?
A justifier par le biais du schéma de principe de l'électrolyse.
Oxydation = anode
Réduction = cathode
Je vous envoie mon schéma de suite en espérant qu'il soit correct.
Pour la question 2, merci davoir reformuler la question, c'est parce qu'il est un bon conducteur de l'électricité ?
Pour la 3, vous voulez dire que je dois annoter le schéma donc ?
Pour la 4, il me semble avoir inversé, l'électrode de graphite correspond à l'anode et la trompette correspond à la cathode.

Bonjour,
1. Le schéma est pas mal mais il manque des informations cruciales telle que les bornes +/- du générateur et donc le sens de déplacement des électrons (primordial pour en déduire où ils seront "arrachés" et "absorbés" tu ne crois pas  ?)
?)
2. Oui c'est ça, et comme c'est un métal conducteur, les électrons vont pourvoir s'y déplacer de façon homogène aisément.
3. Oui ! Cf. mon commentaire sur la question 1. Du sens de déplacement des électrons, tu peux en déduire à quelle électrode a lieu l'oxydation et celle où a lieu la réduction, et donc en déduire où sont l'anode et la cathode.
4. A confirmer avec un schéma complet.

Oui bien sûr il faut que je le complète.
Je renvois de suite mon schéma.
Pour la 5, je dois me référer aux bornes du générateur, donc les électrons se déplacent du - au + de ce dernier.
Pour la 6, le sens du courant est à l'inverse du + au - ; je ne comprends pas ce que cela signifie " une illustration sommaire" pouvez vous m'expliquer ?
De plus, dites moi si mon schéma manque d'informations.

Tu peux t'inspirer du schéma fourni dans la fiche de mon message du 25-02-21 à 17:44 (§II. 1)
Il n'est pas très lisible sinon, je ne sais pas si tu as moyen d'améliorer sa résolution ?
N'est il pas correct ? Car en voyant le schéma fourni de la fiche je trouve que c'est assez similaire.
De plus, ai je bon dans mes réponses ?
Comme je te l'ai écrit, sa résolution ne me permet pas de tout lire (le texte notamment) : tu as effectivement ajouté des flèches devant représenter le sens de déplacement des électrons et l'intensité du courant mais tu n'as pas précisé qui est qui.
Et de ce schéma, comment déduis-tu où a lieu l'oxydation et la réduction ? Et donc où se trouvent l'anode et la cathode ?
J'ai fait du mieux possible ..
Les flèches en gras représentent le sens du courant.
Je le deduis parce que à l'électrode de graphite se produit un dégagement de bulles de gaz ?
Bonjour,
@gbm : Bonjour ! 
@Blackdark : Conseils pour améliorer ce que je suppose être la photo d'un schéma :
a) Orienter l'appareil de manière que le lecteur puisse lire le résultat sans attraper de torticolis.
b) Utiliser pour le schéma une feuille de papier blanc uni et un stylo d'encre noire.
c) Bien éclairer la feuille.
d) Maintenir la feuille perpendiculairement à l'appareil photo.
Bonsoir odbugt1,
Et merci pour la retouche, enfin un schéma lisible  !
!
@ Blackdark : enfin un schéma complet !
Si on fait l'inventaire au niveau de la trompette : il faut effectivement la recouvrir d'atomes d'argent ; comme on a une solution de nitrate d'argent, il faut donc en effet capter des électrons pour régir la demi-équation : Ag+ + e- --> Ag
Il s'agit d'une réduction, c'est donc la cathode !
Il y a donc effectivement une oxydation au niveau de l'électrode en graphique (anode) : quel est le couple en jeu ? Quelle demi-équation électronique régit la transformation ?
Quelle est l'équation-bilan de la transformation ?
Le couple en jeu serait Cu/Cu^2+ ?
La demi équation qui régit serait Ag^+ + e^- = Ag ?
L'équation bilan je dirais Cu + 2Ag^+ = Cu^2+ + 2Ag ?
Je pense m'être emmêlé les pinceaux...
Non ... Applique la fiche ! Il faut faire l'inventaire des couples en jeu, tout en se rappelant qu'on cherche une oxydation :
La trompette est basée sur le cuivre.
Il s'oxyde facilement au contact du dioxygène de l'air et de l'eau. Afin de le protéger, les artisans luthiers doivent procéder à une électrolyse. Cette technique nécessite un générateur, des câbles électriques, une électrode de graphite, des minces en platine et une bassine de solution aqueuse acide d'ion argent et nitrate dans laquelle plongent la trompette et le graphite. La trompette, l'électrode de graphite, le générateur et la solution aqueuse constituent un circuit en série. La bassine présente un dégagement de bulles de gaz sur l'électrode de graphite. Apres un certain temps delta T, l'instrument de cuivre ressort totalement couleur argent. L'aspect et le toucher de l'argenture sont sans aspérités, lisses et homogènes.
Ce n'est pas le couple Cu2+/Cu qui est en jeu pour deux raisons :
- déjà parce qu'on a dit que la trompette est la cathode (= réduction) ; il ne peut donc y avoir d'oxydation ;
- et qu'oxyder le cuivre de la trompette serait une mauvaise idée, puisqu'on cherche justement à le protéger avec de l'argent.
Concentre-toi sur l'électrode en graphite, d'autres indications sont fournies dans l'énoncé (je t'ai mis les informations essentielles en bleu).

Mais non ...
Je te rappelle que - par définition - une réaction d'oxydoréduction est une transformation chimique entre un oxydant et un réducteur de deux couples différents.
On a déjà étudié la cathode (cf. message du 26-02-21 à 19:37), on étudie désormais l'anode (= électrode de graphite).
Que se passe-t-il à ce niveau d'après l'énoncé ? Je t'ai mis en couleur les infos essentielles pour rappel 
A ce niveau des bulles de gaz se forment dans la solution aqueuse au niveau de l'électrode de graphite donc ça serait :
Ag^+NO3^- / AgNo3 ?
A ce niveau des bulles de gaz se forment dans la solution aqueuse au niveau de l'électrode de graphite donc ça serait :
Ag^+NO3^- / AgNo3 ?
Non, Ag+ + NO3- --> Ag n'est pas une oxydation, il n'y a aucun échange d'électron (sans compter qu'une telle réaction est fictive).
Ou peut être O2 / H2O ?
Cela devient déjà un peu plus intéressant
 .
.Mais une oxydation est-elle possible avec un tel couple ?
Pourquoi ne cherches-tu pas à écrire la demi-équation électronique du couple O2/H2O dans le sens de l'oxydation ?
Oui mais tu as écrit l'équation dans le sens de la réduction quand on souhaite une demi-équation d'oxydation.
Ce qui serait plus logique puisqu'on cherche un dégagement gazeux en produit.

Donc 2H2O -> O2 + 4H+ + 4e^- ?
Si cela est correct, je me permets de passer à la question suivante qui est que représentent les ions nitrates vis à vis de la réaction, ça pourrait être qu'ils peuvent s'absorber directement sur le cuivre et le faire se dissoudre ?
Bonjour,
Tout d'abord, je viens de constater que tu as posté le même exercice sur un autre forum, ce qui n'est pas respectueux vis-à-vis de l'aide que je t'apporte depuis le début : ![]() .
.
Je te demanderai donc d'aller poster un message là-bas pour dire que tu reçois déjà de l'aide ici, c'est la moindre des choses, sinon j'arrêterai tout bonnement mon aide.
Si cela est correct, je me permets de passer à la question suivante qui est que représentent les ions nitrates vis à vis de la réaction, ça pourrait être qu'ils peuvent s'absorber directement sur le cuivre et le faire se dissoudre ?
OK pour la demi-équation au niveau de l'électrode en graphite
Il ne faut pas écrire tout ce qui te passe par la tête, on a déjà écrit la demi-équation électronique faisant intervenir le cuivre et l'ion nitrate n'intervenait pas.
Les ions nitrates représenteraient alors vis à vis de la réaction un catalyseur ?
Il n'est pas question de catalyse ici, plus simple la réponse
Bonjour, excusez moi pour cela, j'y vais de ce pas, je n'y pensais plus, mais je n'ai pas posé les mêmes questions, car je ne voulais pas tout mettre ici pour ne pas vous faire perdre trop de temps ...
Je ne vois pas quel rôle peuvent jouer les ions nitrates cependant ils sont solubles dans l'eau.
Etant donné qu'ils ne participent ni à l'oxydation au niveau de l'anode, ni à la réduction au niveau de la cathode, ce sont donc des ions ...

Où vas-tu chercher des truc pareils 
Je te conseille de lire attentivement cette fiche : ![]() Les transformations chimiques
Les transformations chimiques
Dans une transformation chimique, tu as des réactifs, des produits et des espèces spectatrices, tout simplement
Ah oui d'accord, les ions nitrates représentent des espèces spectatrices.
J'ai cherché un peu trop loin ...
Pour la question suivante, l'équation de la réaction serait :
5H + O2 + Ag^+ = 2H2O + Ag + H^+ ?
Ton équation-bilan est fausse, il faut justifier ton équation-bilan sur la base des demi-équations électroniques écrites plus haut :
Ag+ + e- --> Ag
2H2O --> O2 + 4H+ + 4e-
Et les équilibrer avant de les sommer, tout est expliqué dans cette fiche : ![]() [lien]
[lien]
Ag+ + e- --> Ag (je multiplie par 4)
2H2O --> O2 + 4H+ + 4e-
Donc l'équation de la réaction :
4Ag+ + 2H2O = --> 4Ag + O2 + 4H+ ?
De plus, est-il possible que vous m'aidiez sur quelques questions supplémentaires sur ce même sujet ?
Je ne vois pas comment trouver la relation à l'aide du tableau ...
Poste-moi ton tableau d'avancement de la réaction pour que je puisse le vérifier :
 extrait de
extrait de Q05 - Puis-je insérer une image dans mon message ? Comment faire ? Quelle image est autorisée ?
Est ce : n(Ag+) = 4 × n(O2) ?
Ta relation est correcte à condition d'expliquer quelles quantités de matière tu considères (n(Ag+) = ? et n(O2) = ?)
De plus, est-il possible que vous m'aidiez sur quelques questions supplémentaires sur ce même sujet ?
Oui, il va falloir me recopier l'énoncé sans chercher à l'adapter
Mais je n'ai pas les valeurs de leur quantité de matière donc comment remplacer ?
Je vous envoie mon tableau.
Revoici l'énoncé :
La trompette est basée sur le cuivre.
Il s'oxyde facilement au contact du dioxygène de l'air et de l'eau. Afin de le proteger, les artisans luthiers doivent procéder à une électrolyse. Cette technique nécessite un générateur, des câbles électriques, une électrode de graphite, des minces en platine et une bassine de solution aqueuse acide d'ion argent et nitrate dans laquelle plongent la trompette et le graphite. La trompette, l'électrode de graphite, le générateur et la solution aqueuse constituent un circuit en série. La bassine présente un dégagement de bulles de gaz sur l'électrode de graphite. Apres un certain temps delta T, l'instrument de cuivre ressort totalement couleur argent. L'aspect et le toucher de l'argenture sont sans aspérités, lisses et homogènes.
Voici les autres questions :
11) Proposer une relation entre le courant I, la constante de Faraday F, le temps Delta T, l'avancement x de la réaction et le nombre d'electrons mis en jeu.
12) les luthiers ont pour habitude de laisser une épaisseur de 4.2 micromètres d'argenture sur le cuivre. La trompette dépliée fait une surface totale de cuivre valant 0.8 m^2. Déterminer l'expression puis la valeur de la quantité de matière d'argent ainsi déposée sur le cuivre de l'instrument.
13) estimer en conséquence le temps Delta T nécessaire à la réalisation d'une telle argenture.
14) la première acidité est forte entre l'acide sulfurique et l'ion hydrogénosulfate. Quelle est la conséquence et la signification de cette relation.
15) quelle est, en se basant sur les domaines de prédominance, l'espèce majoritaire de l'acide sulfurique pour un pH = 6.07 ?
16) déterminer la concentration des espèces : ions oxonium, ions hydrogénosulfate et ion sulfate présentes dans le milieu.
17) Proposer l'équation bilan de réaction de corrosion du cuivre en milieu oxygéné comme l'air.
Pour la question 11 j'ai trouvé I ×delta T = X × n(e^-) × F
Pour la 12 pouvez vous me mettre sur la voie car je n'ai aucune idée de comment faire ... J'ai quelques données donc la masse molaire et la masse volumique de l'argent, est ce que cela me sera utile à cette question ?

Mes remarques concernant ton tableau d'avancement : il faut définir tes notations
n= ?
E = ?
x = ?
C = ?
S = ?
Pour les questions suivantes je te laisse y réfléchir, les principales notions à utiliser sont dans les deux fiches fournies au début de l'échange
Jai lu les fiches et je ne comprends toujours pas comment faire pour la question 12, quelle formule dois je utiliser ?
Dans ce cas il faut expliquer que n = quantité de matière initiale en ions Ag+.
OK pour le "en excès" pour l'eau, mais à éviter pour l'ion H+.
Concernant la question 11 :
Pour la question 11 j'ai trouvé I ×delta T = X × n(e^-) × F
Il faut expliquer ce que tu fais ! Le jour du bac, un résultat fourni sans justification ce sera 0. Que signifient F ? X ?
Question 12 :
les luthiers ont pour habitude de laisser une épaisseur de 4.2 micromètres d'argenture sur le cuivre. La trompette dépliée fait une surface totale de cuivre valant 0.8 m^2
De l'énoncé, tu peux en déduire le volume d'argenture nécessaire V = S * e
S = surface totale de la trompette
e = épaisseur d'argenture
Puis si on te fournie la masse volumique de l'argent, tu peux en déduire la masse et donc la quantité de matière finale en argent nécessaire pour cette transformation forcée.
Attention aux unités !

Pour la question 11 je n'ai pas précisé car chaque lettre est défini dans l'énoncé.
Pour la 12 donc, d'abord on fait V = E × S
Soit 4,2 micrometres × 0,8 m^2 ; donc 4,2 × 10^-6 × 0,8 = 3,36 × 10^-6 m^3.
Ensuite masse = masse volumique × volume donc 10,49 g . cm ^3 × 3.36 × 10^-6 m^3 donc 10.49 × 10^-2 × 3.36 × 10^-6 soit 3.525 × 10^-7 g/m^-3.
Ensuite n = m/M donc (3.525 × 10^-7) / 108 g / mol ^1 donc 3.3 × 10^-9 moles ?
Je pense m'être un peu embrouillé ...

 moteur de recherche
moteur de recherche page de choix du forum
page de choix du forum fiches du site
fiches du site