Inscription / Connexion Nouveau Sujet
Électrozingage avec anode soluble
Bonsoir, j'ai besoin d'aide avec un TP que j'ai à finir :
Comment réaliser la galvanisation d'un métal pour le protéger de l'oxydation ?
Voici le protocole (raccourci, juste ce qu'il est important) :
- 150 ml de solution de sulfate de Zinc à 1,0*10^-1 mol.L-1
-Relever les masses des lames de fer et de zinc. (J'ai trouvé mzinc=11,63g et mfer=11,13g)
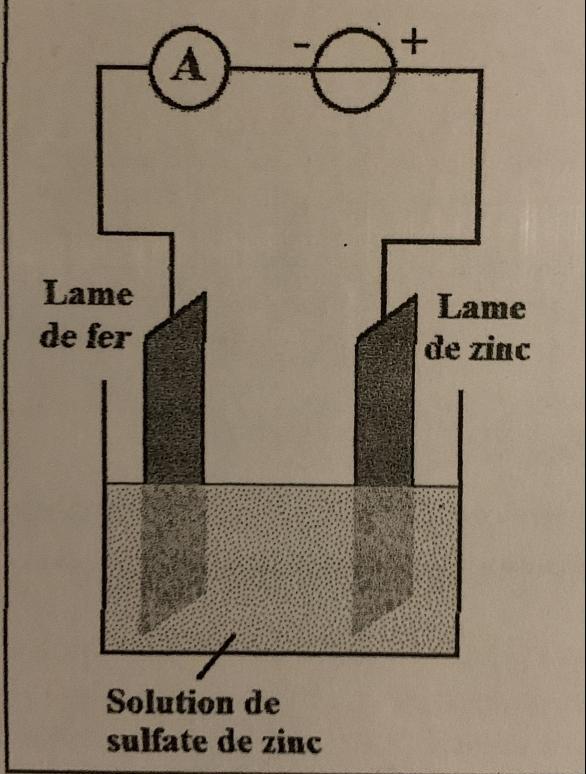
-Mettre les lames dans la solution et les relier à un générateur avec ampèremètre
-allumer le générateur avec I=0,10A
-Faire une électrolyse de 20min
-Noter la durée exacte de l'électrolyse et celle de l'intensité du courant I.
-Sécher les lames et les peser (j'ai trouvé mfer=11,17g mais je n'ai pas noté mzinc, devrais-je trouver pareil ou plus qu'à la première pesée ?)
Données Zinc :
Masse volumique zinc : 7,13 g.cm-3
Couple : Zn2+/Zn
M(Zn)=65,4g.mol-1
Voici les questions :
1. Calculer et comparer les variations de masse mdelta(Zn) et mdelta(Fe) des lames de zinc et de fer.
2. Reproduire le schéma de l'électrolyseur. Indiquer le sens de circulation des électrons puls en déduire la demi-équation électronique se produisant à chaque électrode.
3. En utilisant la durée de l'électrolyse et l'intensité du courant électrique, retrouver la masse de zinc déposée sur la lame de fer.
4. A partir de la masse de zinc et des dimensions de la surface de la couche de zinc déposées sur la lame de fer, évaluer l'épaisseur de la couche de zinc déposée sur la lame.
Conclusion: justifier l'expression e électrolyse à anode soluble »
Pour la première je ne sais pas...
Merci d'avance
J'ai fait ceci :
mdeltazinc=0,04g c'est correcte ?
Qu'est ce que j'étais censé trouver pour mdeltafer puisque je ne l'ai pas pesé ? Je veux dire une plus grosse masse ou moins grosse qu'à la première pesée ?


