Inscription / Connexion Nouveau Sujet
dosage par étalonnage d'une solution coloréee
bonjour a tous, je suis nouveau sur ce site et j'aurais besoin de votre aide s'il vous plait.. je bosse depuis cette après midi sur cette exercice et je n'avance pas du tout.. je n'arrive pas a cerner les différentes questions :
nous avons une courbe A (axe y) et lambda ( en nm) ( axe x ). de 350 nm a 423... il y a un sommet qui atteint 0,1 A et il descend jusqu'à l'axe des abscisses et c'est constant jusqu'à 500 nm et ça remonte jusqu'à 640 nm pour 0.95 A et ça descend en pente jusqu'à 700 nm. Donc :
1 ) A partir du spectre d'absorption du bleu patenté V, déterminer la longueur d'onde lambda de travail ( je pensais à 640 car maximal mais il faudrait justifier car je ne sais pas quoi dire  , c'est a dire la radiation monochromatique pour laquelle on va mesurer l'absorbance des 6 solutions étalons. Justifier ce choix. Faire le lien entre la couleur de la solution et la longueur d'onde de travail. Je n'arrive pas du tout a cerner cette question donc vous pourriez m'aider s'il vous plait ? merci <3
, c'est a dire la radiation monochromatique pour laquelle on va mesurer l'absorbance des 6 solutions étalons. Justifier ce choix. Faire le lien entre la couleur de la solution et la longueur d'onde de travail. Je n'arrive pas du tout a cerner cette question donc vous pourriez m'aider s'il vous plait ? merci <3
2) Également rappeler quelles précautions sont à prendre pour l'utilisation des cuves du colorimètre. Le colorimètre offre le choix entre les longueurs d'onde suivantes : 655 nm ; 585 nm ; 565 nm ; 470 nm. Quelle est celle qu'il faut choisir pour optimiser les mesures ? argumenter les réponses. on règle le zéro du colorimètre (faire le ''blanc'') : rappeler comment on doit procéder et l'utilité ce ce réglage. Je ne sais pas quoi répondre notamment dû au colorimètre car je ne sais pas ce qu'est c'est, j'ai cherché mais je ne vois pas du tout comment savoir les nm et comment rappeler comment on doit procéder..
3) nous avons un tableau qui fait pour chaque solution est de 1 à 6 et pour chaque A : 0.08 ; 0.11 ; 0.18 ; 0.35 ; 0.68 ; 1.01. tracer la courbe d'étalonnage : A=f(C). J'ai vu et ça vérifie la loi de beer lambert mais je ne sais pas comment '' établir l'équation numérique qui la traduit ''.
Merci vraiment pour l'aide que vous m'apporter  j'espère que vous pourriez m'aider car je suis perdu et vous êtes mon seul recours. Ce que je demande, c'est juste des explications pour que je comprenne lorsque vous répondrez aux questions et encore merci les amis
j'espère que vous pourriez m'aider car je suis perdu et vous êtes mon seul recours. Ce que je demande, c'est juste des explications pour que je comprenne lorsque vous répondrez aux questions et encore merci les amis 
Pas même quelqu'un s'il vous plait ?  je perd espoir.. j'y travaille pour essayer d'avancer mais je nage complètement ! aidez moi
je perd espoir.. j'y travaille pour essayer d'avancer mais je nage complètement ! aidez moi 
salut  !
!
1) effectivement d'après ta description ça colle. Tu serais donc donc les rouges. Ta solution est de quelle couleur? Et tu conclues
2) tu sais ce qu'est la spectrophotométrie? à quoi correspond la cuve?
Salut Shadowmiko!!!
Eh bien non je ne sais pas exactement.. j'ai mener des recherches mais je ne comprends pas trop son utilité.. c'est pour ça que je voudrai que vous m'aidiez pour les 3 questions et que vous m'expliquiez pourquoi avoir mis cette réponse pour que je comprenne votre raisonnement.. j'ai essayé de le faire chez moi mais je ne vois pas quoi répondre donc si vous pourriez répondre au 3 questions en m'indiquant a quoi correspond les réponses ça serait vraiment sympathique .. merci a tous 
ce que je veux c'est pas que vous me fassiez l'exercice mais un max d'infos pour que j'arrive à la réponse et ce que j'aimerai c'est des gros textes, a la forme d'une argumentation... ça serait vraiment génial de votre part a tous
Bonne nuit !! 
1) je t'ai déjà donné les pistes pour celle là. Tu es dans le domaine du rouge. De quelle couleur est ta solution? Tu as un lien évident entre les deux couleurs
je pensais que c'était bleu puisque la solution est du absorption bleu patenté V.
je ne comprend rien.. explique moi pour tout la question 1 qui est :
1 ) A partir du spectre d'absorption du bleu patenté V, déterminer la longueur d'onde lambda de travail, c'est a dire la radiation monochromatique pour laquelle on va mesurer l'absorbance des 6 solutions étalons. Justifier ce choix. Faire le lien entre la couleur de la solution et la longueur d'onde de travail.
je ne vois pas de lien dit moi stp
j'ai encore du mal pour ces question, vous pourriez me donner les réponses en m'expliquant pourquoi cette réponse et pour quel question vous répondez svp :
enfin.. mettez moi sur la bonne voie quoi .
- nous avons un tableau qui fait pour chaque solution est de 1 à 6 et pour chaque A : 0.08 ; 0.11 ; 0.18 ; 0.35 ; 0.68 ; 1.01. tracer la courbe d'étalonnage : A=f(C). J'ai vu et ça vérifie la loi de beer lambert mais je ne sais pas comment '' établir l'équation numérique qui la traduit ''.
- Également rappeler quelles précautions sont à prendre pour l'utilisation des cuves du colorimètre. Le colorimètre offre le choix entre les longueurs d'onde suivantes : 655 nm ; 585 nm ; 565 nm ; 470 nm. Quelle est celle qu'il faut choisir pour optimiser les mesures ? argumenter les réponses. on règle le zéro du colorimètre (faire le ''blanc'') : rappeler comment on doit procéder et l'utilité ce ce réglage. Je ne sais pas quoi répondre notamment dû au colorimètre car je ne sais pas ce qu'est c'est, j'ai cherché mais je ne vois pas du tout comment savoir les nm et comment rappeler comment on doit procéder..
- A partir du spectre d'absorption du bleu patenté V, déterminer la longueur d'onde lambda de travail, c'est a dire la radiation monochromatique pour laquelle on va mesurer l'absorbance des 6 solutions étalons. Justifier ce choix. Faire le lien entre la couleur de la solution et la longueur d'onde de travail.
1) tu m'as bien dit qu'il y avait un pic non? ce serait plus simple si tu joignais les graphiques. Après si la solution est bleue c'est que le bleu est émis et non absorbé
Beer-Lambert : A = f(C). Si c'est proportionnel c'est juste A = kC c'est tout
Cuves colorimètre : tu ne dois pas mettre les doigts sur les faces lisses, seulement sur les faces striées. Pour faire le blanc tu places de l'eau distillée dans la cuve, et tu réalises les mesure. Ensuite tu considères que le résultat de cette mesure est "zéro" : tu étalonnes quoi
longueur d'onde de travail : ben tu as donné une piste 
désole shadowmiko je ne peux pas, on a pas de courbe c'est un texte.. mon prof est un tueur.. il nous casse la tête.. il dit qu'il faut qu'on se matérialise la courbe..
je vous remets les différentes questions pour que vous reprenez tous ça dans l'ordre car les différentes réponses m'embrouilles ^^ c'est fou mais je vous remercie tout de même pour votre générosité
nous avons une courbe A absorbance (axe y) et lambda ( en nm) ( axe x ). de 350 nm a 423..il y a un sommet qui atteint 0,1 A et il descend jusqu'à l'axe des abscisses et c'est constant jusqu'à 500 nm et ça remonte jusqu'à 640 nm pour 0.95 A et ça descend en pente jusqu'à 700 nm. Donc :
1 ) A partir du spectre d'absorption du bleu patenté V, déterminer la longueur d'onde lambda de travail ( je pensais à 640 car maximal mais il faudrait justifier car je ne sais pas quoi dire , c'est a dire la radiation monochromatique pour laquelle on va mesurer l'absorbance des 6 solutions étalons. Justifier ce choix. Faire le lien entre la couleur de la solution et la longueur d'onde de travail. Je n'arrive pas du tout a cerner cette question donc vous pourriez m'aider s'il vous plait ? merci <3
2) Également rappeler quelles précautions sont à prendre pour l'utilisation des cuves du colorimètre. Le colorimètre offre le choix entre les longueurs d'onde suivantes : 655 nm ; 585 nm ; 565 nm ; 470 nm. Quelle est celle qu'il faut choisir pour optimiser les mesures ? argumenter les réponses. on règle le zéro du colorimètre (faire le ''blanc'') : rappeler comment on doit procéder et l'utilité ce ce réglage. Je ne sais pas quoi répondre notamment dû au colorimètre car je ne sais pas ce qu'est c'est, j'ai cherché mais je ne vois pas du tout comment savoir les nm et comment rappeler comment on doit procéder..
3) nous avons un tableau qui fait pour chaque solution est de 1 à 6 et pour chaque A : 0.08 ; 0.11 ; 0.18 ; 0.35 ; 0.68 ; 1.01. tracer la courbe d'étalonnage : A=f(C). J'ai vu et ça vérifie la loi de beer lambert mais je ne sais pas comment '' établir l'équation numérique qui la traduit ''.
1) tu as la bonne hypothèse. ta solution est bleue et absorbent donc dans les domaines que tu cites.
2) je te l'ai dit, c'est à propos des doigts
3) c'est simplement A = k*C
OK donc pour la 1) c'est la valeur maximal donc que c'est 640 et on est dans les rouges c'est ca ? et la solution est bleu car c'est bleu patenté V . pourquoi on prendrait la valeur maximale = 640 nm et non la valeur minimal = 210 nm alors que ce qu'on veut c'est la longueur d'onde lambda de travail ? Mais quel lien on peut faire entre la couleur rouge et bleu de la solution ? je ne vois pas, expliquer moi svp .. 
pour moi c'est 655 nm car c'est proche de 640 mais pourquoi ? je ne sais pas ^^ expliquez moi aussi 
aidez moi je vous en supplie. je suis perdu 
c'est le rouge et le vert non ? mais je ne vois pas pourquoi ça fait un lien.. et pourquoi il faut prendre la valeur max 640 nm et non la valeur min 210 nm car ce qu'on veut c'est la longueur d'onde de travail.
a la question 2 ) pour moi c'est la réponse de 655 nm car c'est proche 640 nm mais je ne sais pas pourquoi c'est lui qu'il faut prendre .. donc tu pourrais me le dire stp ?

donc tout d'abord j'aimerai ta confirmation pour les autres questions est ce possible ?
1) c'est 640 nm car c'est maximal mais pourquoi on prendrai pas la minimal d'absorption pour la longueur d'onde de travail qui est 210 nm mais plutôt 640 nm? également je ne vois pas de lien entre la couleur rouge du 640 nm et celui de la solution patenté qui est bleu.. pourrais tu m'expliquer ?
2) je répondrai 655 nm car c'est proche de 640 nm mais je ne sais pas pourquoi il faut vraiment prendre cette longueur d'onde.. il dise d'argumenter et je ne sais pas quoi dire..
3) la réponse est loi de beer lambert est vérifier donc équation a = k(c) ou y = ax+b ?
il faut trouver k ? ou a et b ?
merci
1) Oui, c'est bien 640 nm. C'est en cette longueur d'onde de travail que ta solution absorbe le plus : quelque chose y est donc sensible. Pourquoi pas 210 nm ? Eh bien il s'agit d'une longueur d'onde émettant dans l'UV, que déduis-tu ?
2) Pour les précautions, shadowmiko te l'a expliqué. Et oui, c'est 655 nm. Il faut que ta longueur d'onde soit le plus proche possible du pic d'absorbance afin de limiter au maximum l'incertitude sur ton calcul du dosage.
3) Si tu as une relation de proportionnalité c'est que A = kC. À toi de déterminer la valeur de k.
je sais pas ... j'en déduit que en dessous de 400nm c'est de l'ultraviolet donc que c'est pas bon alors que 640 nm c'est dans le domaine visible.. si c'est pas ça fait en moi part stp  merci a tous
merci a tous
c'est vrai.. vraiment un gros merci.. vous être trop cool.. mais je ne vois toujours pas trop le lien entre le rouge et la couleur de la solution patenté V qui est bleu mdr^^ vous pourriez pas me le dire en m'expliquant ?... MERCI
enfaite si je crois car tous deux est dans le domaine visible non ? je crois pas trop que ça soit mdr^^
Si les feuilles sont vertes c'est qu'elles absorbent toutes les couleurs sauf le vert. Qu'en déduis-tu ?
je me demande quand même : as-tu vu les synthèses additives et soustractives? Tu n'as pas réagit lorsque je t'ai parlé de la complémentarité des couleurs...
évidemment c'est exact  mais je n'ai rien compris.. ma prof explique vraiment très mal donc je ne sais pas trop quoi répondre pour le lien qu'il y a entre le rouge et la solution bleu patenté V .. peut être que comme c'est rouge c'est car il absorbe le bleu et le vert donc sauf le rouge et pour le bleu c'est qu'il absorbe le rouge et le vert donc sauf le bleu et ça n'émet que du blanc pour les deux quelque chose du genre non ?!!
mais je n'ai rien compris.. ma prof explique vraiment très mal donc je ne sais pas trop quoi répondre pour le lien qu'il y a entre le rouge et la solution bleu patenté V .. peut être que comme c'est rouge c'est car il absorbe le bleu et le vert donc sauf le rouge et pour le bleu c'est qu'il absorbe le rouge et le vert donc sauf le bleu et ça n'émet que du blanc pour les deux quelque chose du genre non ?!! 
non si la solution est bleue c'est qu'elle émet cette couleur. Donc elle absorbes les couleurs complémentaires :
et
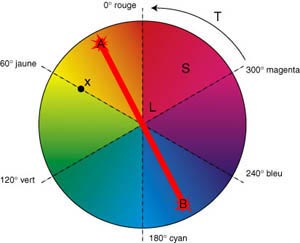
je complète (nombre restrictif d'images jointes par message)
Lorsqu'un objet est éclairé par une lumière blanche (contenant toutes les couleurs) incidente, celle-ci peut-être absorbée, réfléchie ou diffusée dans toutes les directions ou transmise si l'objet n'est pas opaque.
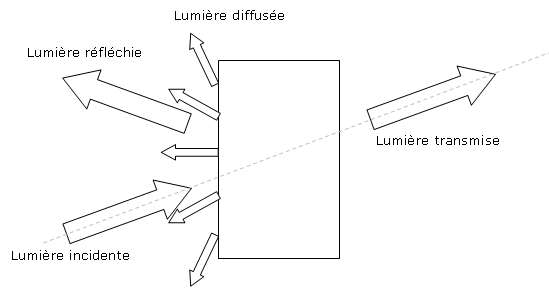
La couleur perçue de l'objet dépend de la synthèse des lumières reçues par l'il.
Un objet qui n'absorbe rien diffuse toutes les radiations visibles et apparaît blanc.
Un objet qui absorbe tout le rayonnement visible ne diffuse rien et apparaît noir.
Enfin un objet coloré absorbe une partie du spectre visible. Le spectre de la lumière diffusée par cet objet correspond au spectre complémentaire du spectre de la lumière absorbée (spectre d'absorption).
L'exemple super classique est le drapeau français éclairé en lumière blanche :
 (j'ai choisi un drapeau français stylé)
(j'ai choisi un drapeau français stylé)
La partie bleue du drapeau absorbe le spectre de la lumière correspondant à sa couleur complémentaire (le jaune).
La partie blanche n'absorbe aucune radiation et diffuse en totalité le spectre de la lumière blanche.
Enfin la partie rouge du drapeau absorbe le spectre de la lumière correspondant à sa couleur complémentaire cad le spectre dont la couleur perçue est le cyan (cyan = bleu).
OK merci pour ce petit cours a vous deux ..  donc en gros faut que je dise ça :
donc en gros faut que je dise ça :
La couleur rouge qui est émit par la longueur d'onde absorbe le spectre de la lumière correspondant à sa couleur complémentaire c'est-à-dire le spectre dont la couleur perçue est le bleu.
c'est ça le lien ?
ok donc :
La couleur bleu qui est émit par la longueur d'onde absorbe le spectre de la lumière correspondant à sa couleur complémentaire c'est-à-dire le spectre dont la couleur perçue est le rouge.
c'est ca ?
ouais. Normalement c'est le orange, mais ce sont deux couleurs très proches sur le spectre et surtout on ne connait pas l'intensité du bleu
OK j'hésitais un peu de dire orange aussi mais comme on parlais de rouge et de bleu.. je ne voulais pas trop sortir du sujet et être hors sujet mdr^^ merci à vous deux j'ai d'autres questions vous pourriez m'aider svp ? merci à vous deux
A partir d'une solution mère So de concentration Co = 1,0.10puissance-4 mol.L-1, on veut préparer les 6 solutions suivantes :
on a 6 solutions en tout nomme S1 S2 S3 S4 S5 S6 et dont la concentration molaire C (mol.L-1) qui correspond à 2,0.10puissance -6 (s1), 3,0.10puissance -6 (s2), 5,0.10puissance -6 (s3), 1,0.10puissance -5 (s4), 2,0.10puissance -5 (s5), 3,0.10puissance -5 (s6).
ce qu'on veut trouver nous c'est son volume Vo de solution mère à préparer (mL) mais je ne sais pas quoi faire. aidez moi je vous en supplie
2)b) faire la liste du matériel nécessaire a la préparation de l'ensemble de ces solutions. décrire, de manière précise, le protocole expérimental permettant de fabriquer la solution n°2.
3) que représente l'ensemble de ces six solutions colorées ? justifier la réponse .
4) dans les mêmes conditions expérimentales, la solution d'alondont a une absorbance Aa = 0,10
déterminer, si possible, de deux manières différentes, la concentration molaire Ca inconnue en bleu patenté V de la solution d'Alodont
en déduire son titre massique tA.
données : masse molaire atomique (g.mol-1) : C : 12,0 ; H : 1,0 ; O : 16,0 ; N : 14,0 ; S : 32,1 ; Ca : 40,1
pour la 3) j'aurais dit dilution mais je ne sais pas comment argumenter enfin justifier la réponse.. vous pourriez m'aider ? et pour la 4) c'est n = C x V enfin.. je crois mais je n'est rien compris donc aidez moi s'il vous plait.. Pour finir la question 2) sur les matériels et le protocole expérimentale.. je n'ai rien compris du tout...
(re)merci
2)b) tu fais une dilution donc pipettes jaugées, fioles jaugées et béchers
3) une échelle de teinte, tu dois voir que ta solution devient de plus en plus claire
4) tu as le coefficient k de Beer-Lambert?
non pas encore car je ne l'ai pas encore calculé désolé ^^ mais c'est quoi le protocole expérimentale de la question 1 pour faire la solution 2 ? j'ai essaye de le faire tout a l'heure mais rien ne vient en tête ..
également merci pour les matériels mais tu pourrais me dire pour chaque quel est leurs fonction.. ? en gros ce qu'ils servent exactement pour la création de ces différents solutions.. je suis complétement perdu.. tu es génial shadowmiko 
OK merci et pour ton truc du bêcher.. il servira a quoi exactement car les autres instruments que tu m'as cité sont les principaux non ? a moins qu'on prend les produits dont a besoin pour la mettre dans le bêcher et qu'en suite on prend la pipette jaugé pour prendre ce qu'on a besoin pour la mettre dans la fiole jaugé c'est ca non?
mais je ne vois pas trop pour la question 4) tu peux m'expliquer
Dans les mêmes conditions expérimentales, la solution d'alondont a une absorbance Aa = 0,10
déterminer, si possible, de deux manières différentes, la concentration molaire Ca inconnue en bleu patenté V de la solution d'Alodont
en déduire son titre massique tA.
oui ce sont les principaux mais il faut prélever la solution mère quelque part
4) tu n'as aucune autre indication? une courbe? etc.
oui c'est vrai. il faut bien la prélever quelque part mdr^^
et non je n'ai pas de courbe.. désole. ma prof est une vicieuse et elle pose toujours des questions super dure auquel il faut se mettre a plusieurs pour trouver la réponse.. j'en peu plus .. j'ai super mal à la tête là ^^
Y'a bien un "si possible"
#Le titre massique c'est la concentration massique
tA = m/V = (n*M)/V = (n/V)*M = c*M
Or c = n/V avec n = m/M
#Pour la deuxième manière c'est avec la loi de Beer-Lambert
A = k*C = 0,10
Et pour tout te dire la question 4 c'est la plus chaude ..encore les autres ça aller un petit peu car je trouver les réponses sans vraiment avoir complété et d'autres ou c'était la misère. j'étais complétement perdu et grâce a vous j'ai mieux compris mais pour cette question 4.. c'est super énervant. elle fait des trucs qu'on a jamais vu et même si on l'a vu.. on comprenait rien donc ça revenait a jamais l'avoir vu.. tu vois le truc mdr^^ ?
OK mais je ne vois pas trop quelle formule vraiment prendre car je ne sais pas pourquoi la concentration molaire etc.... je ne trouve rien du tout de tout ça .. pour la question 4)
et pour le protocole expérimentale ? pourquoi il parle de la solution n°2 en particulier ? les autres sont différentes.. donc ça veut dire que le protocole est différent pour cette solution donc que ce que tu m'as donner est faux ?
je suis perdu avec tous ces trucs .. je n'en peu plus là





