Inscription / Connexion Nouveau Sujet
Domaine de prédominance
bonjour ,
voici l'énoncé du sujet :
Un litre de solution d'engrais pour plantes a été préparé en dissolvant 0.10 mol de phosphate d'ammonium (NH4)3PO4 solidde dans une quandtité suffisante d'eau. L'équation correspondante s'écrit :
(NH4)3PO4 ==> 3NH4+ + PO43-
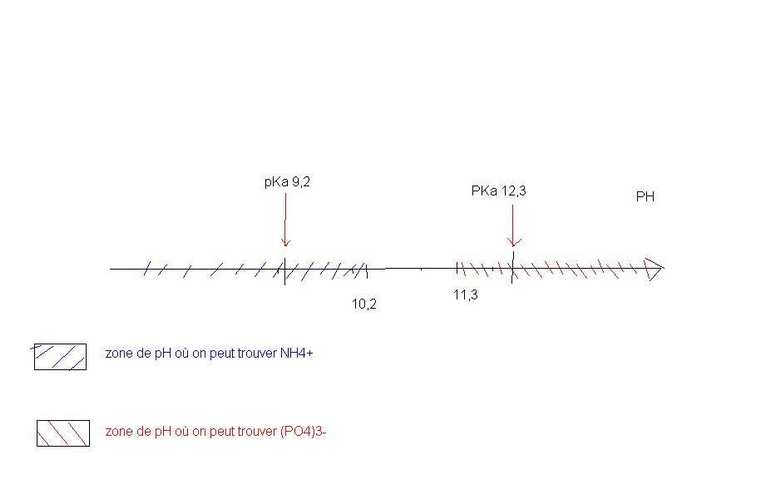
1) placer sur un meme axe gradué en pH les domaines de prédominances des espèces acides et basiques des 2 couples concerné (données : PKA1 (NH4+/NH3)=9.2 et PKA2 (HPO42-/PO43-)=12.4
je pense que j'ai juste a cette question
2)existe t_il un intervalle de pH où les ions ammoniums et phosphates prédominent tous les 2 ? pourront-ils coexister dans la solution d'engrais ?
- déja il y a l'acide et la base du phosphate sont tous les 2 des ions lequel prendre ?
- sur mon axe , il y a NH3 et HPO42- qui prédominent tous les 2 or NH3 n'est pas un ion ...
POurriez vous m'aider....
les espèces concernées par la question sont NH4+ et PO43-.
Il n'y a pas de domaine de coexistence commun pour ces ions
les ions NH4+sont négigeagles devant NH3 pour pH>pka+1=10,2 et les ions PO43-sont négligeables devant les ions HPO42-pour pH<pKa-1=11,3
Merci beaucoup . En fait je ne vois pas la rapport entre les deux parties de a question : il n'y a pas d'intervalle où il prédomine tous les 2... mis je ne vois pas ee quoi cela nous montre qu'il coexisteront ou pas dans la solution d'engrais ...?
Oui j'ai trouvé le meme axe :donc , puisque il n'y a pas d'intervalle où ces deux ions prédominent , il ne pourront pas coexister dans la solution d'engrais si j'ai tout bien compris ?? Mais je vois pas comment justifier cela !! C'est une évidence !!