Inscription / Connexion Nouveau Sujet
DM de physique/chimie
Bonjour à tous, j'aurais besoin d'aide pour terminer mon DM.
L'énoncé est joint.
Voici mes réponses :
I.
1. Je trouve bien c0=6.0 mol/L en faisant c0= P /MNaHooù P est le pourcentage massique de NaHO. Par contre pour la rédaction...
/MNaHooù P est le pourcentage massique de NaHO. Par contre pour la rédaction...
2. Pas de problème. On prélève 1/100 de solution où l'on rajoute 99/100 d'eau distillé étant donné qu'il s'agit d'une dilution de 100. Pour la matériel : pipette jaugée, fiole jaugée...
3. H3O+(aq) + HO-(aq) [url] 2H2O(l).
2H2O(l).
II.
1. v =  (2gh+v0²).
(2gh+v0²).
2. h = v²/2g.
3. v =  2(h'-h)g)
2(h'-h)g)
Merci de votre aide !
*** edit T_P : pas de scan de documents ***
Voici l'énoncé :
I Déboucheur d'évier.
Sur une bouteille de déboucheur d'évier, on lit l'indication suivante : "Pourcentage massage en hydroxyde de sodium : 20%". On cherche à vérifier cette indication.
On considérera le déboucheur comme une solution aqueuse d'ydroxyde de sodium uniquement, qu'on appellera S0, de concentation molaire notée c0. La densité du déboucheur d'évier est d = 1.2.
A partir de cette solution S0, on prépare une solution S1 de concentration c1 = c0/100. On prélève V1 = 20.0 mL de solution S1, que l'on place dans un bécher. On dispose par ailleurs d'une solution d'acide chlorhydrique SA, de concentration cA = 0.100 mol/L. On ajoute progressivement de la solution SA à la solution S1 okacée dans le bécher, en notant V le volume de solution SA ajouté. Pendant cet ajout progressif, on mesure la conductivité  de la solution en notant, pour chaque valeur de V, la valeur de
de la solution en notant, pour chaque valeur de V, la valeur de  .
.
Les conductivités molaire ioniques et les couples acido-basiques ainsi que les masses molaires atomiques se trouvent sur le document joint.
1. Montrer que si l'indicatoin de l'étiquette est axacte, on doit avoir c0=6.0 mol/L. Dans les questions suivantes, on fera comme si cette concentration était exacte.
2. Décrire un protocole chiffré permettant de fabriquer, à partir de S0, 1.00L de solution S1.
3. Ecrire l'équation de la réaction qui a lieu lorsqu'on ajoute la solution SA à la solution S1.
4. Il arrive un moment on a apporté juste assez de solution SA pour consommer tous les ions hydroxyde initialement présents dans le bécher. Déterminer V à ce moment-là. On le notera Vé.
5. Déterminer littéralement, puis numériquement, les concentrations des ions en solution en fonction de V lorsque cette réaction se produit encore, c'est-à-dire lorsqu'il reste des ions hydroxyde dans le bécher, c'est-à-dire pour V < Vé. On pourra s'aider d'un tableau d'avancement.
6. En déduire l'équation de la courbe  =f(V) pour V < Vé.
=f(V) pour V < Vé.
7. On continue d'apporter de la solution SA. Déterminer littéralement, puis numériquement, les concentrations des ions en solution en fonction de V. Cette fois, on a V > Vé.
8. En déduire l'équation de la courbe  =f(V) pour V > Vé.
=f(V) pour V > Vé.
9. Tracer la courbe  =f(V) pour V allant de O mL à 25 mL.
=f(V) pour V allant de O mL à 25 mL.
10. Montrer que la connaissance de l'abscisse du point remarquable de la courbe permet de calculer c1.
11. En réalité, l'expérience a donné pour l'abscisse du point remarquable la valeur Vexp=10.8 mL. Calculer la valeur de c1, puis celle de c0, correspondantes. En déduire le pourcentage massique en hydroxyde de sodium de la bouteille. S'est-on fait arnaquer ?
II Tarzan.
Tarzan, accroché à une liane tendue pendant d'une branche, s'élance d'un rocher en se donnant une vitesse initiale 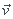 0, perpendiculaire à la liane. Au plus bas de son mouvement, son centre d'inertie est à une hauteur h en-dessous de sa position de départ.
0, perpendiculaire à la liane. Au plus bas de son mouvement, son centre d'inertie est à une hauteur h en-dessous de sa position de départ.
On notera m la masse de Tarzan et g l'intensité de la pesanteur.
1. Déterminer la vitesse de Tarzan lorsqu'il passe à la position la plus basse de son mouvement.
2. Déterminer l'altitude maximale que Tarzan pourra atteindre de l'autre côté.
3. S'il veut atteindre le rocher d'en face, situé à la hauteur h', quelle vitesse initiale v0 doit-il avoir ?
Mes réponses se trouvent au-dessus de ce message.


