Inscription / Connexion Nouveau Sujet
diagramme de distribution d espece acido-basiques...
Bonjour esce que quelqu'unn pourrias m'aider s'il vous plait...
1. L'acide hypochloreux a pour formule HOCl(aq) . Sa base conjuguée CIO-(aq) est appelée ion hypochlorite.
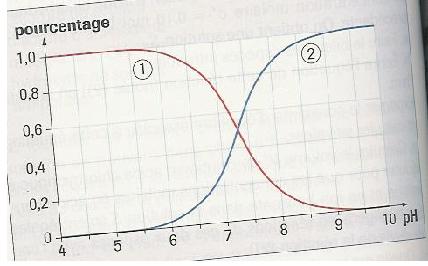
Le document ci-dessous représente les pourcentages des espèces chimiques acide et base du couple HOCl(aq)/CIO-aq) en fonctio du pH pour une solution telle que:
c=[HOCl(aq) ] + [CIO-(aq)]=1.00x10-2mol.L-1
a) En quel point a-t-on HOCl(aq)=CIO-(aq)?
En déduire le pKa du couple HOCl(aq)/CIO-aq).
là j'ai mis: HOCl(aq)=CIO-(aq) quand la courbe 1 er 2 se coupent...?et le pKa je sais pas...
b) Sur un axe gradué en pH , placer les domaines de prédominance des espèces acide et basique du couple. Justifier votre réponse.
c) Identifier les 2 courbes 1 et 2.
la courbe 1 c'est l'acide:HOCl(aq)
et la 2 c'est la base:CIO-(aq)
d) Ecrire l'équation de la réaction de l'acide hypochloreux avec l'eau.
HOCl + H2O -> ClO- + H3O+
2.a) Ecrire l'aquation de la réaction de l'acide hypochloreux avec l'ion hydroxyde.
HOCl + HO- -> ClO- + H2O
b) Calculer la constante d'équilibre associée à l'equation de cette réaction.
Conclure.
K= [ClO-] / [HOCl][HO-] mais apès je fais comment??
Donnée
Produit ionique de l'eau: Ke=1.0x10-14 à 25°C
Meric beaucoup...
a) je pense que le pka est le pH au point d'intersection car il n'y a pas d'éspèce prédominante
b) acide d'un coté et base de l'autre sur un axe de pH avec la frontière au pKa ( 7 et d brouettes )
c) ok
d) ok
2) a) ok
b) L'astuce je pense est de multiplier K par [H30+]/[H3O+] ainsi ca se simplifie avec le Ke et tout......


