Inscription / Connexion Nouveau Sujet
Déplacements d'électrons en chimie organique
Bonjour à tous !
Alors voilà, je comprends les déplacements des doublets d'électrons au cours du mécanisme réactionnel en chimie organique mais, je ne vois pas pourquoi on se retrouve avec parfois avec des ions avec une charge complète positive ou négative.
Je vous ai joint un exemple de ce que je ne parviens pas à comprendre. Comment se fait-il que l'atome d'azote devienne un ion N+ ? Et que Cl devienne Cl- ? Pareil pour les atomes d'oxygènes de la deuxième réaction...
Si quelqu'un pouvait m'aider à comprendre, ce serait super !
Merci d'avance 
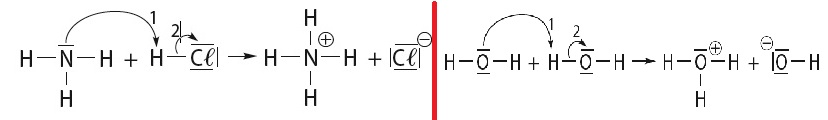
Bonsoir
Je pense que c'est une histoire de covalence.
L'atome d'azote fait 3 liaisons normalement. Dans ta première réaction, tu vois qu'il va chercher un hydrogène, ce qui l'oblige à faire 4 liaisons. Il a donc une liaison de plus que la normale, d'où un +.
La liaison qu'il y a entre le Chlore et l'hydrogène se casse. L'azote va chercher un H+ en gros... et les électrons de la liaison HCl vont revenir sur l'atome le plus électronégatif (celui qui attire le plus les électrons), à savoir le Cl. Celui-ci va donc se retrouver avec des électrons mais sans faire de liaison...d'où la charge négative.
Pour la deuxième réaction, c'est pareil. L'oxygène peut faire deux liaisons. Dans ta réaction, il va chercher un H, formant ainsi 3 liaisons (d'où le +) et les électrons de la laison OH reviennent vers le O (plus électronégatif que le H), d'où le - sur OH-.
Je ne sais pas si j'ai bien expliqué mais si tu n'as pas compris dis moi.
Merci pour votre réponse !
Mais, dans la première réaction, l'atome d'azote après avoir fait 4 liaisons autour de lui possède bien 8 électrons donc 1 en plus que d'habitude ! Ça devrait donc être un - mais c'est un + qu'il porte !
Je ne comprends pas très bien...


