Inscription / Connexion Nouveau Sujet
demi équivalence
Bonjour, quelqu'un pourrait -il m'expliquer pourquoi à la demi équivalence, dans le cadre du dosage d'un acide on a (AH) = (A-)
S'il vous plaît??
Bonjour,
Si tu doses ton acide par une base alors à l'équivalence tu n'as plus d'acide. Pourquoi ? Parceque justement tu as introduit la quantité "équivalente" de base pour que [AH] = 0.
Donc la demi-équivalence c'est quoi ? c'est donc le moment où la concentration en acide ne vaut plus que sa moitié initiale. Et c'est logique que [AH] = [A-] a ce moment là car [AH] diminue d'autant que [A-] augmente.
Si tu préfères les maths:
[AH]demi_eq = [AH]ini / 2
Par conservation de la matière:
[A-]instant_t = [AH]ini - [AH]instant_t
Donc a fortiori au moment de la demi_eq:
[A-]demi_eq = [AH]ini - [AH]demi_eq = [AH]ini / 2 = [AH]demi_eq
Salut !
!
Juste un complément
D'une manière générale, on se sert de la demi-équivalence pour les solutions tampons.
Lors du titrage d'un acide faible par une base forte ou inversement, on se retrouve dans le cas d'une solution tampon (les quantités de matière d'acide et de base conjuguée sont identiques). La faible variation de pH lors de l'ajout d'une base forte correspond à un effet tampon.
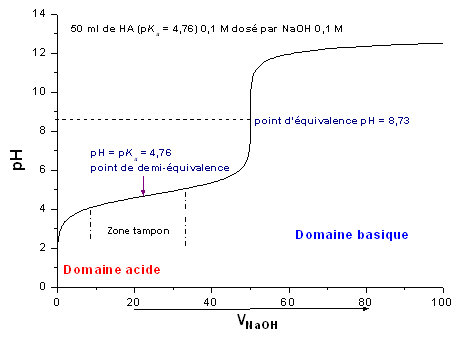
Le point (ou pH) de demi-équivalence correspond à
pH = pKa