Inscription / Connexion Nouveau Sujet
correction d'un exercice 1
bonjour,
j'ai un exercice à faire en DM et je voudrais savoir si mes résultats vous parraissent correctes, merci d'avance d'y consacrer un peu de temps ! ( je n'ai pas détaillé tous mes calculs ! )
voici l'énoncé :
On s'intéresse ici au titrage d'un volume Va=20.0 mL d'une solution d'acide propanoïque C2H5COOH par une solution d'hydroxyde de sodium de concentration Cb=1.00.10^-2 mol.L.
On donne le pka du couple C2H5COOH/C2H5COO- : pka=4.9.
a) ecrire l'équation de titrage.Calculer la constante d'équilibre associée.
réponse :
C2H5COOH + OH- = C2H5COO- + H2O
K = Ka / Ka' = 10^(pka' - pka)
=10^14.0-4.9
= 1.3.10^9
On donne le volume versé à l'équivalence : Vbe=14.0 mL
b)déterminer les concentration molaire c et massique t de la solution.
réponse: a l'équivalence on a n(C2H5COOH) = n(OH-)
d'où C = (Cb*Vbe)/ Va = 7.00.10^-3 mol.L
t = C*M(C2H5COOH) = 7.00*10^-3*74 = 5.2.10^-1 g.L
c)Quelle est la quantité d'ions OH- a-t-on apportée lorsque Vb=5 mL.
réponse : n(OH-) = CbVb = 5.10^-5 moles
d)sachant que pour Vb=5 mL on a pH=4.4 , en déduire la quantité d'ions OH- présents dans la solution.
La réaction peut elle etre considérée comme totale ?
réponse :
pH=pka+log[OH-] d'où [OH-] = 10^(ph-pka)
=10^4.4-14.0
=2.5.10^-10 mol.L
donc nf(OH-)=[OH-]*(Va+Vb) = 6.3.10^-12 moles
Vb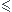 Vbe donc OH- est limitant d'où
Vbe donc OH- est limitant d'où
xmax = n(Oh-)= CbVb = 5.00.10^-5 mol
or nf(OH-) = CbVb - xeq d'où xep= CbVb - nf(OH-)
=4.9.10^-5 mol
T = xeq/xmax = 98% la réaction est presque totale.

 !
!

