Inscription / Connexion Nouveau Sujet
Concentration par spéctrophotométrie
Bonjour, je fais appel à vous pour un exercice de chimie, en voici l'énoncé :
On cherche à déterminer la concentration du colorant de Tartrazine et de bleu Patenté V dans un sirop par spectrophotométrie.
On réalise les expériences suivantes à partir du sirop dilué 10fois, d'une solution S1 de Tartrazine à c1= 2.00*10^-2 g/L et d'une solution S2 de bleu patenté V à c2=1.00*10^-2 g/L. A l'aide d'un spectrophotomètre avec des cuves de largeur l=1cm, en obtient des courbes donnant l'absorbance A en fonction de la longueur d'onde.
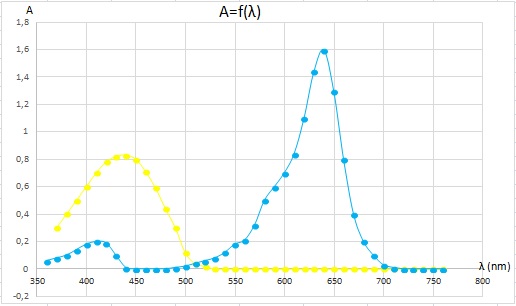
1) Tracer sur un graphe les spectres des deux colorants grâces aux données fournies,quelle est la couleur de la solution de tartrazine.
La solution absorbe dans le 450 nm, donc le violet dont la couleur complémentaire est le jaune.
2)On effectue un mélange d'un même volume V de S1 et S2, donner les concentrations.
On mélange par le même volume, les concentrations sont divisées par deux mais celle de tartrazine reste deux fois supérieurs à celle de bleu patenté.
De même pour c2
3) L'absorbance est proportionnelle à la concentration de l'espèce colorée donner le lien entre et
(absorbance du colorant dans le mélange), de même pour
et
, de même pour
4)L'absorbance étant additive donner la relation entre A (absorbance du mélange) et
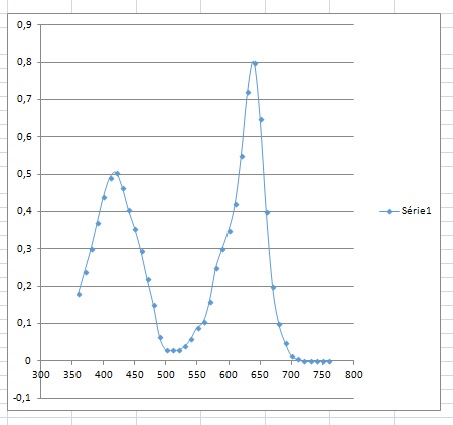
5) Tracer le spectre du mélange et prévoir sa couleur.
Le mélange absorbe dans le rouge et le violet, de couleur complémentaire bleue et jaune, par synthèse soustractive le mélange est vert.
6) On a un tableau avec pour la Tartrazine, =425nm,
=50
, de même pour le bleu avec 360nm et 180
, que représentes ces valeurs.
Ce sont la longueur d'onde pour laquelle l'absorbance est maximale ainsi que le coefficient d'absorption.
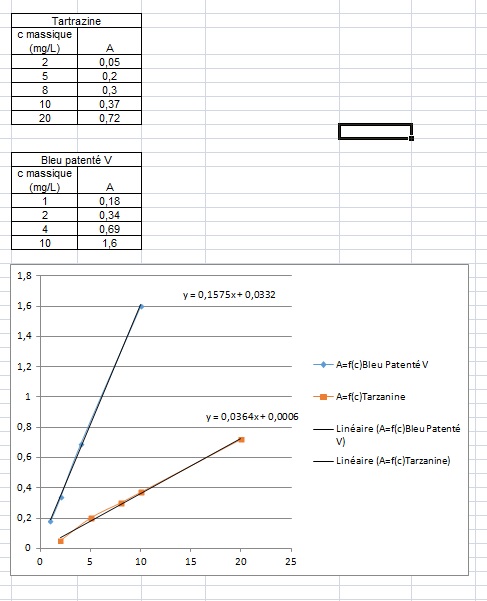
7) Peut on retrouver les valeurs de grâce à une courbe d'étalonnage, on donne pour la tartrazine certaine concentration et leur absorbance associée, de même pour le bleu. De quoi dépend
Il suffit de tracer la courbe A=f(c), le coefficient directeur correspond à .
Puisque, il dépend de A, l, et c.
8) Retrouve t-on grâce au spectre les valeurs précédemment données ?
Oui car grâce aux spectres pour chacun des colorants, l'absorption maximale correspond au lambda donné précédemment.
9)On a fait une échelle de teinte à partir des solutions des colorants, on mesure l'absorbance de chaque solutions à l'aide du spectrophotomètre en se plaçant à =450nm pour la tartrazine et 640nm pour le bleu. Pourquoi choisit-on de se placer à
=450nm plutôt que 420nm pour réaliser le dosage par étalonnage pour la tartrazine dans le mélange ?
10)Déterminer la concentration massique des colorants jaune et bleu dans le sirop dilué, en déduire les concentrations massiques de la tartrazine et du bleu dans le sirop.
11) Pourquoi est-il préférable d'effectuer en général les courbes d'étalonnage A=f(c) à
Et j'ai du mal pour les dernières questions, merci beaucoup.
Salut  !
!
Ce serait bien de voir tes tracés. En outre tu as souvent résolu qualitativement (c'est très bien) mais on te demande aussi des valeurs 
9) A quoi correspondent les valeurs ? C'est dit dans ton énoncé. Donc pourquoi faire ça quand tu sais que tu réalises un dosage ? N'oublie pas que tu as tartrazine et bleu patenté dans le lot
10) Il te faut une résolution graphique selon moi, d'où ma première remarque
11) Que dit la loi de Beer-Lambert ? Quelle est la relation qui est donnée dans cette loi ?
Bonjour et merci d'avoir répondu, voici respectivement les graphes de l'absorbance en fonction de la longueur d'onde (en bleu pour le bleu patenté et jaune pour la tarzanine), celui du mélange des deux colorants, ainsi que les courbes A=f(c) avecles valeures quei ont permi de les tracer qui sont données par l'énoncé.
9) Je vois seulement que c'est fait pour avoir une échelle de teinte...
11) Les spectres UV-Visbles indiquent les valeurs aux maxima d'absorptions, qui sont donc pour une
qui est utilisé dans la loi de Beer Lambert
Merci encore 
9) Tu dois considérer une longueur d'onde telle que l'absorbance de la tartrazine soit proche du max. Mais tu dois faire attention au fait que l'absorbance du bleu patenté soit proche de 0. Et ce sont les conditions que tu retrouves à 450 nm. Si tu te places à 420 nm l'absorbance de la tartrazine est conséquente (même mieux), mais celle du bleu patenté n'est malheureusement pas négligeable.
10) Tu as trouvé ?
11) oui
J'ai une courbe annexe que je n'avais pas prise en compte, il s'agit de la courbe du sirop dilué , il y a deux bandes, une en 425nm pour une absorbance de 1, et une autre à 630nm pour une absorbance de 1.1.
Selon la loi de Beer Lambert, , or l=1 donc
, selon les valeurs données dans l'énoncé
et
?
Cette concentration est dans le sirop dilué fois, pour retrouvé la concentration dans le sirop on les multiplie par 20 ?
D'accord merci beaucoup.
Si ça ne vous dérange pas je me pose quelques questions, comment se fait-il qu'avec les courbes a=f(c), je trouve quand même un assez différent de ce qui est donné, de même qu'à mieux y relire, il y a écrit, de quel paramètre dépend
, alors que dans son expression de la loi de Beer Lambert, il ne peut pas dépendre que d'un paramètre ?
6) Pour être un peu plus précis, j'ai dis que correspondait au coefficient d'absorption, ici il est exprimé en
, donc il s'agit du coefficient d'absorption massique (pour un
qui correspond au
donné) ?
Pour le coup je re-vérifie, quelque chose m'a peut être échappé.
Pour répondre à ta question, ε est le coefficient d'extinction molaire, et s'exprime en L.mol−1.cm−1.
L'absorptivité molaire (c'est son autre petit nom, je te le mets volontairement car tu peux le trouver) dépend de la longueur d'onde, de la nature chimique de l'entité et de la température.
D'accord merci beaucoup.
Justement je me demandais si lorsqu'il est exprimé en , on appelle ça le coefficient d'extinction molaire, est-ce qu'il est juste d'appeler ça le coefficient d'extinctions massique lorsqu'il est exprimé en
, comme dans le cas de l'exercice ?
Donc il s'agit une erreur de l'énoncé puisqu'il est supposé qu'il y a un seul paramètre auquel dépend ?
Hmmm oui parce-que n = m/M et que tu exprimes bien le résultat en fonction d'une masse.
Ils demandent juste de quoi dépend ε donc si c'est écrit au singulier, oui c'est un peu bizarre
Sinon j'ai re-vérifié, je n'ai peut être pas les yeux en face des trous mais ça me semble vraiment ok


