Inscription / Connexion Nouveau Sujet
c'est ce que j'ai fait mais c'est pour n(02) je vois pas comment faire car on connai pas m02
d'accord mais cela ne sert pas pour calculer la quantité de matiere de O2
Attends je suis pas encore là!! Tu m'a dit quetu y arrivait pas pour déterminé les quantités de matière de l'état initial et maintenant tu dis que ta fais ca , Ok alors dit moi comment tu as fait pour la quantité de matière de O2 ?
ba c'est ce que j'essaie de trouver mdr!
on utilise la formule n=m/M M=32 mais m aucune idée
LOL!! on utilise pas cette formule pour calculer la quantité de matière de O2! On te dit dans l'énoncé qu'il y a 1.50 litre de dioxygène, donc on utilise QUELLE FORMULE d'après toi ? ( avec des volumes çà ne te dit rien ?)
x max je vois pas et le reactif limitant c'est pas le dioxygene ?
ba ca fait 0.20-x et 6.25*10-2-x
ensuite je fait quoi?
Comment tu trouves çà?
Il faut utiliser l'éqaution de départ de ta toute première question sinon comment veut tu faire si tu n'a pas l'équation bilan de départ ? Tu comprend au moins ?
Non il faut que tu trouve : pour l'éthanol 0.05-xmax et pour le dioxygène (6.25*10-2)-3xmax à l'état final
Ok ? 
on trouve x superieu ou egal 0.020 et x superieur ou egal a 0.05 nn?
on prend la valeur la plus petite donc xmax= 0.020
Pour l'éthanol : xmax = 0.05 par contre je ne suis pas daccord avec toi pour le dioxygène, comment trouves tu 0.02?



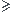 3x
3x

