Inscription / Connexion Nouveau Sujet
Cinétique chimique
Bonjour
J'aurais besoin d'aide pour cet exercice à rendre vendredi
L'énoncé :
Potentiels normaux des couples redox : E0(Zn2+/ Zn)= -0,76V et E0(H3O+/H2)=0,00 V
Volume molaire dans les conditions de l'expérience : V0= 24 L/mol
Masses molaires en g/mol : Cl:35,5;H:1 ; O: 16 ; Zn: 65,4
On étudie la cinétique de la réaction naturelle entre 2 couples. A t= 0,on introduit une masse m= 1g de zinc en poudre dans un ballon contenant V= 40 mL d'une solution d'acide chlorhydrique de concentration Ca= 0,5 mol /L .On recueille le gaz dihydrogène formé au cours du temps et on mesure concentration Ca = 0,5 mol /L .
On recueille le gaz dihydrogène formé son volume V(H2) . A chaque instant ,on designe par x le nombre de mol d'acide disparu et par CR sa concentration molaire résiduelle .
1. Écrire l'équation bilan de la réaction .
2. a) Tenant compte des données numériques de l'énoncé et de l'équation précédemment écrite ,établir les relations: et CR= 0,5-25x.
(x est en mol , V(H2) en L et CR en mol /L )
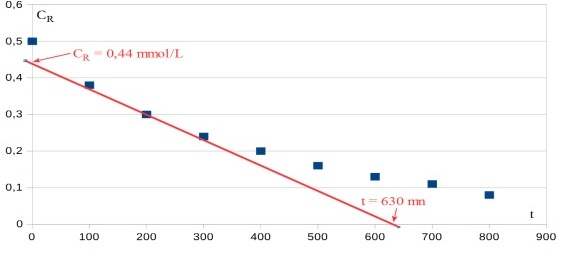
b) Compléter le tableau de mesures ci-dessous et tracer la courbe CR= f(t).
3. a) Déterminer la vitesse moyenne de disparition de H3O+ entre t1= 200mn et t2= 500mn .
b) Déterminer graphiquement la vitesse instantanée de disparition des ions hydronium V(H3O+) à la date t1= 200 min .
4. a) Déterminer la concentration C1 de la solution en ion Zn2+ à t= 300min.
b) Déterminer la concentration C2 de la solution en ion Zn2+ en fin de réaction et calculer la masse mr de zinc restant .
5. Établir une relation entre les vitesses instantanées de disparition de H3O+ et de formation de Zn2+ et en déduire la vitesse instantanée de formation de Zn2+ à t1= 200min .
Bonjour beugg.
Où en es-tu ?
Commence par écrire chacune des demi-équations electroniques associées aux couples rédox concernés.
Déduis ensuite l'équation de la réaction entre le zinc et les ions hydronium et dresse alors le tableau d'avancement.
À toi.
Bonjour picard
On avait raté ce devoir de maison à cause de manque de temps et d'autres raisons...
Mais ensuite on a reçu une correction un peu partielle.
L'équation : 2H3O++ Zn ---> H2+2H2O + Zn2+
2. b) on a complété le tableau ainsi :
| x(mol) | 0 | 4,8 | 8 | 10,4 | 12 | 13,5 | 14,8 | 15,6 | 16,8 |
| CR(mol/L) | 0,5 | 0,38 | 0,3 | 0,24 | 0,2 | 0,16 | 0,13 | 0,11 | 0,08 |
Merci

Le tableau ne colle pas bien il laisse en toute la 2 ; la 3èmecolonne et les deux dernières colonnes
Voici :
x(en mol): 0; 4,8 et 15,6; 16,8
CR(mol/L): 0,5 ; 0,38 et 0,11; 0,08
Jusque là, c'est bon, avec effectivement x en mmol.
Qu'est-ce qui t'arrête ensuite ?
Trace la courbe CR = f(t) et revois, si nécessaire, les définitions relatives aux vitesses de disparition d'un réactif (moyenne et instantanée).
Oui je dois tracer CR= f(t)
Mais concernant l'échelle ,est-il cohérent d'écrire par exemple :
1cm correspond à 0,1 mol/ L ?
Mais concernant l'échelle ,est-il cohérent d'écrire par exemple :
1cm correspond à 0,1 mol/ L ?
Personnellement, j'aurais pris 2 cm pour 0,1 mol/L...
Mais cela n'a pas grande importance.
3.a)
Vm= 1,8.10-5mol/min
-l'unité : il s'agit de mmol.min-1 (voir ta remarque dans un précédent post).
-la valeur : l'application numérique donne 1.86666... on est donc plus près de 1.9 10-8 mol.min-1.
b/
V(t)= -dn/dt
Dérivée d'une constante n'est pas nulle ?
Tu dois donc tracer la tangente à la courbe CR(t) à t = 200 min et évaluer le coefficient directeur de cette tangente.
D'après l'énoncé...
3. a) Déterminer la vitesse moyenne de disparition de H3O+ entre t1= 200mn et t2= 500mn .
Il me semble que tu te trompes de dates...
On a donc Vm=(13,5-8)/(500-300)= 1,83.10-2 mmol/min ?
Oui effectivement...
Mais ce n'est pas obligatoire de convertir cette valeur (vitesse moyenne) en mol/min?
j'aurais voulu aussi savoir si le type de calculer la vitesse instantanée de disparition d'un réactif par le graphe est le même que par le calcul
Merci bonne nuit 
Mais ce n'est pas obligatoire de convertir cette valeur (vitesse moyenne) en mol/min?
3.b)
2cm --> 200min
10cm --> 0,5 mol/L
V(t=200)= (0,5-0)/(200-0)= 2,5.10-3L
2° chose, ce n'est pas ce que je trouve.
v(t = 200 min) = -dn / dt = - V dCR / dt
numériquement : v(t = 200 min) = -40 10-3
 [(0 - 0.44) 10-3 / (630 - 0)]
[(0 - 0.44) 10-3 / (630 - 0)]
soit, finalement : v(t = 200 min) = 2.79 10-8 mol.min-1
j'aurais voulu aussi savoir si le type de calculer la vitesse instantanée de disparition d'un réactif par le graphe est le même que par le calcul
Les résultats obtenus par la méthode graphique dépendent beaucoup du soin apporté au tracé de la tangente à la courbe à la date à laquelle on veut trouver la vitesse.
Le 2.5 que tu avais obtenu n'est pas très éloigné du 2.79 que j'ai eu (10% d'écart entre nos deux valeurs quand même !), mais ce qui ne va pas dans ton calcul, c'est la puissance de 10...
OK ?
Oui c'est OK merci 
4. a)
2H3O+ +Zn --> H2+H2O +Zn2+
(n(H3O+)/2)disp.= n(Zn2+)
Or n(H3O+)= 10,4.103 mol
<==>
C1= 5,2.10-3/40.10-3
C1= 0,13 mol/L
Si les calculs sont corrects ensuite comment calculer mr?
Peut-on écrire mr= CRV*M
Il a l'air ne pas aller car le x là ?
Pour la dernière question 5/
V(H3O+)/2= V(Zn2+)
Or VZn2+(t=200min)= 2,79.10-8 mol/min
V(Zn2+)= 1,3.10-8 mol/min
Tout ceci est-il correct ?
Merci 
4. a)
2H3O+ +Zn --> H2+H2O +Zn2+
(n(H3O+)/2)disp.= n(Zn2+)
Or n(H3O+)= 10,4.103 mol
C1= 5,2.10-3/40.10-3
C1= 0,13 mol/L
4.b)
À la fin de la réaction :
n(Zn2+)f= 16,8.10-3/2= 8,4.10-3 mol
C2= 0,2 mol /L
Dans ce cas, H3O+ étant le réactif limitant, on aura xmax = 20 10-3 mol
nmax(Zn2+) = xmax / 2 = 10 10-3 mol
et C2 = 10 10-3 / 40 10-3 = 0.25 mol.L-1
Je ne sais pas laquelle des deux réponses est effectivement attendue, relis attentivement l'énoncé.
Enfin, pour la 5)...
V(H3O+)/2= V(Zn2+)
Super
Oui c'est à la fin de la réaction
Mais je comprends pas bien comment vous avez trouvé :
xmax= 20.10-3 mol
Merci 
Le tableau d'avancement est...
| valeurs en mol | 2 H3O+ | + | Zn | = | Zn2+ | + | H2 | + | 2 H2O |
| t = 0 | 20 10-3 | 15.3 10-3 | 0 | 0 | Excès | ||||
| en cours | 20 10-3 - x | 15.3 10-3 - x/2 | x/2 | x/2 | Excès | ||||
| t final | 20 10-3 - xf = 0 | 15.3 10-3 - xf/2 | xf/2 | xf/2 | Excès |
La réaction s'arrête quand le réactif limitant (càd H3O+) a disparu
 20 10-3 - xf = 0 soit : xf = 20 10-3 mol.
20 10-3 - xf = 0 soit : xf = 20 10-3 mol.Merci Picard c'est clair
Pour calculer la masse restante :
mr= mi-md
md= nd * M = 0,01*65,4= 0,654g
mr = 1- 0,654= 0,346 g
C'est bon ?




