Inscription / Connexion Nouveau Sujet
chimie minerale
Bonjour
Énoncé:
1/ on dispose au laboratoire, une solution So de chlorure de calcium (cacl2) de concentration co=1 mol/L de volume vo=1 L
1/1 déterminer la masse mo de A utilisée pour préparer so.
1/2 écrire l équation de dissolution de A dans l eau
2/ a partir de so, on prepare une solution s1 ,decimolaire c1=0,1 mol/L, de volume V1=100 cm^3
2/1 determiner le volume de so, a prelever vp pour preparer s1
2/2 indiquer le mode operatoire (materiels,verrerie)
2/3 calculer le facteur de dilution k
2/4 en deduire le volume Ve d eau distille utilise pour preparer s1
3/ on preleve V'1 =50mL de s1 .on melange ce volume de s1 a une solution S2 de chlorure de sodium ,de volume v2=30 mL et de concentrations c2=0,3 mol/L .on obtient une solution s3
3/2 determiner la concentration molaire de ces especes
3/3 ecrire la relation d electroneutralite
3/4 montrer que s3 est une solution neutre
3/5 en deduire le pH de s3 .donner sa valeur a 25°c
4/ on ajoute a s3 une solution S4 de nitrate d argent (agNO3)
De concentration c4=10^-2 mol/L et de volume V4 =10 ml.on obtient. Un precipite blanc qui noircit a la lumiere
4/1 indiquer la nature de ce precipite
4/2 ecrire l equation bilan de la reaction de precipitation .
4 3 determiner la masse du precipite
Reponse
Question 1/1
mo=Co*Mo*Vo
mo=1*111*1
mo=111 g
Question 1/2
Question 2/1
J ai besoin d aider
Merci d avance pour votre aide
.
Bonsoir,
I.
Question 1 :
OK mais comme je te l'ai déjà expliqué il faut un minimum de rédaction !
Question 2 :
Attention :
En effet, on met des majuscules aux espèces chimiques
Pour la partie II, il s'agit d'un protocole de dilution classique, c'est à savoir refaire sans hésitation : ![]() [lien]
[lien]
Je ne lirai ta proposition que si tu respectes le format de rédaction proposé dans la fiches :
Solution mère :
...
...
Solution fille :
...
...
L'ajout d'eau ...
Ainsi ...
Solution mère : solution so de Cacl2 de concentration co=1 mol/L
VP: volume de solution a prélever
Solution fille: solution diluée s1 de concentration c1=0,1 mol/L
De volume V1=100 cm^3
L ajout d eau ne modifie pas la quantité de matière de soluté
On donc
Co*Vp=C1*V1
VP=(C1*V1)/Co
100 cm ^3=0,1 L
VP=(0,1*0,1)/1
VP=0,01 L
Prélever a l aide d une pipette de
volume V1 de la solution mère.
Introduire dans une fiole jaugée de volume vp de la solution prélevé, VP
Compléter a l aide d une pissette avec de l eau distillée jusqu'au trait jaune
homogénéiser la solution après avoir boucher
Question 2/3
Co: désigné la concentration de la solution mère
C: désigné la concentration de la solution fille
F={co)/c
F=1/0,1
F=10
Question 2/4
J ai besoin d aider
Tu recommences à faire du flood 
Concernant la question 2 : il faut détailler davantage, tout comme la fiche le fait
Question 3 : OK
Question 4 : tu as le volume de solution mère à prélever, quelle quantité d'eau distillée faut-il ajouter pour atteindre le volume de la solution fille ?
N'importe quoi ... Tu ne réponds pas du tout à la question posée :
2/4 en déduire le volume Ve d'eau distillée utilisé pour préparer s1
Franchement : tu prélèves un volume Vp de la solution mère, tu dilues la solution en introduisant un volume Ve d'eau distillée, tu obtiens donc la solution fille V1.
Ve = ?
Vé=V1-Vp
Ve=0,1-0,01
ve=0,09 L
Oui !
Pour la partie 3, il faut faire un schéma de la situation avec :
- les deux solutions avant le mélange (avec pour chacune d'elles les concentrations des espèces en présence, ainsi que le volume de chaque solution) ;
- la solution obtenue après mélange : Vtot = ...
Je te laisse y réfléchir ...
Bonjour gbm.
J aimerais que vous verifier mon devoir de dissertation sur l île histoire géographie
Je t'ai expliqué que je n'interviendrai plus car ce que tu as proposé ne relève nullement d'une dissertation, tout au plus un paragraphe argumenté de collège : il faut absolument que tu regardes des fiches de méthode pour savoir gérer ce type d'exercice et regarder quelques exemple sur le net
OK,je vous comprends
Pardonne moi pour mes erreurs, mais je dois rendre le devoir demain
Je vous en supplie encore 😢
Je veux bien poursuivre avec toi sur l'exercice de chimie (qui est l'objet de ce sujet) et pour lequel j'espère te faire progresser. Pour ce qui est du sujet d'histoire, je laisse shadowmiko te faire un retour puisqu'elle a pris la suite de l'échange avec toi
Bonsoir
Solution so
CaCl2===> Ca^2+ + 2 Cl^-
Solution s1
CaCl2 ====> Ca^2+ + 2Cl^-
La concentration des espèces chimiques.
[Ca^2+]= (n(CaCl2)/VP+V1
[Ca^2+]= Co*VO/VP+V1
[Ca^2+]=(1*0,01+0,1*0,1)/0,01+0,1
[Ca^2+]=0,18 mol/L
[Cl^-]=(4nCl^-)/vp+V1
[Cl^-]=(2*Co*VP+2*C1*V1)/VP+V1
[Cl^-]=(2*0,01+2*0,1*0,1)/0,11
[Cl^-]=0,36 mol/L
Le volume de chaque solution
Solution so
VP=0,01L
Solution s1
V1=0,1 L
La solution obtenue après le mélange
NaCl===> Na^+ . Cl^-
Vtot=Vp+V1+V'1+V2
Vtot=0,01+0,1+0,05+0,03
Vtot=0,19 L
Où est le schéma demandé ?
Où sont les explications avec des phrases ?
Je ne comprends pas ce que tu fais
Fais un effort ... Propose-moi quelques chose.
Tu n'as qu'à regarder les sujets déjà traités dans lesquels j'ai proposé ce type de schéma
Bonjour,
Exemple de schéma possible :
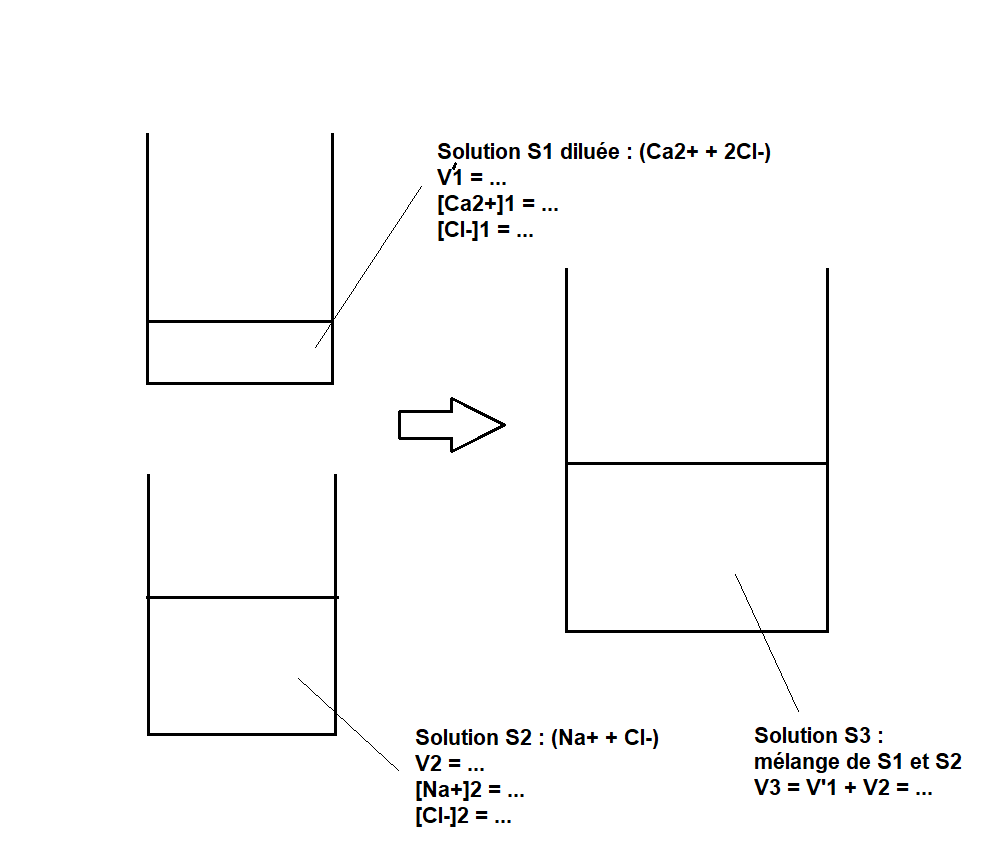
Son intérêt est de définir toutes les notations employées et préciser toutes les données importantes de l'énoncé.
Désormais je te laisse réfléchir à la partie 3, avec un minimum de rédaction pour justifier ce que tu écris avec des formules ...

Voici ma proposition
Solution mère: solution s1 de concentration c1=? et de volume v'1=50 ml
Solution fille: solution dilue de concentration c2=0,3 mol/l et de volume v2=30 ml
L ajout d eau ne modifie pas la quantité de matière
C1*V'1=C2*V2
C1=(C2*V2)/V'1
C1=0,18 mol/l
[Ca^2+]=0,1225 mol/l
Bonsoir,
1 semaine après, tu n'as toujours pas renseigné le schéma que je t'ai proposé ...
D'autre part, je ne comprends pas pourquoi tu cherches à déterminer une concentration C1 qui est fournie dans ton énoncé ...
Bref, il n'y a aucune dilution à refaire (c'était l'objet de la partie 2), il faut juste raisonner sur les équations de dissolution du chlorure de calcium (S1) et du chlorure de sodium (S2) dans l'eau.
On s'occupera du mélange (S3) dans un deuxième temps ...
Absence de rédaction et de schéma, quand tu nous tiens 
Bonjour
[Ca^2+]=n(Ca^2+)/V'1+V2
[Ca^2+]=(1*0,05)/0,08
[Ca^2+]=0,0625 mol/l
[cl^-]=(2n(cl^-)+C2*V2)/V'1+V2
[Cl^-]=0,2375 mol/l
[H3O^+]=10^-7 mol
[HO^-]=10^-7 mol
[Na^+]=n(Na^+)/V'1+V2
[Na^+]=0,1125 mol/l
Bonjour,
Bonjour
[Ca^2+]=n(Ca^2+)/V'1+V2
[Ca^2+]=(1*0,05)/0,08
[Ca^2+]=0,0625 mol/l
[cl^-]=(2n(cl^-)+C2*V2)/V'1+V2
[Cl^-]=0,2375 mol/l
[H3O^+]=10^-7 mol
[HO^-]=10^-7 mol
[Na^+]=n(Na^+)/V'1+V2
[Na^+]=0,1125 mol/l
Pas de rédaction => je ne lis plus tes propositions.
Désormais c'est soit tu suis nos conseils, soit je m'arrête-là
Question 3/2
Solution 1
CaCl2 ==> Ca^2+ + 2 Cl^-
Solution 2
Nacl ===> Na^+ +cl^-
Solution s3
V3=V'1+V2
Calculons la concentration de ca^2+
[Ca^+]=n(Ca^2+)/V3
Avec n(Ca^2+)=n(cacl2)
Et n(cacl2)= C1*V'1
C1: désigné la concentration de la solution s1
V'1: désigné le volume de la solution s1
Finalement
[Ca^2+]=(C1*V'1)/V3
C1*V'1=0,1*0,05 et V3=0,08
[Ca^2]=(0,1*0,05)/0,08
[Ca^2+]=0,0625 mol/l
Tu es sacrément entêté, je n'ai toujours pas eu le schéma maintes fois demandé et complété :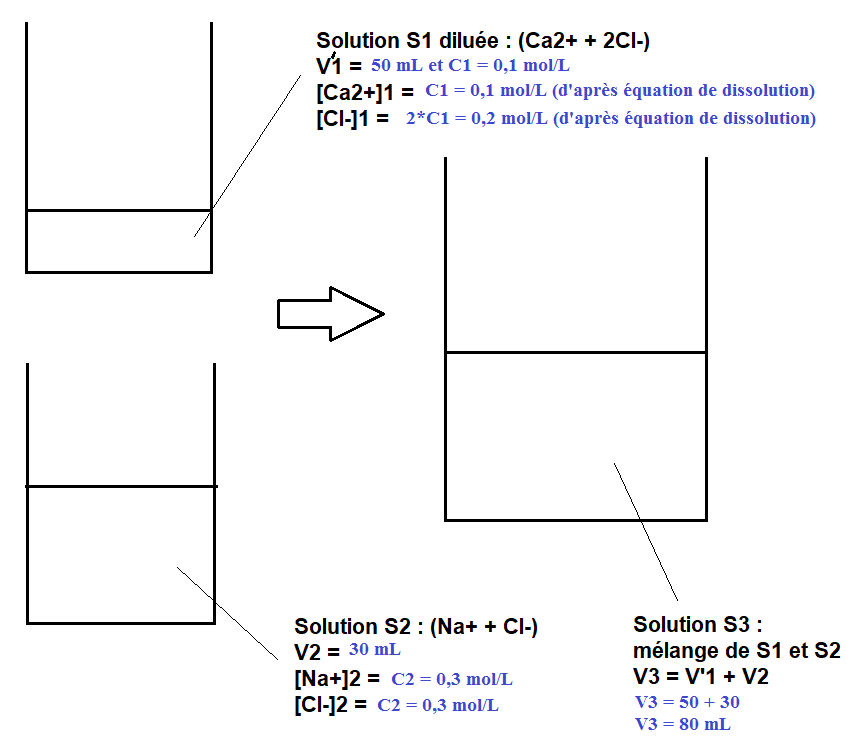
Pour déterminer ensuite les concentrations finales, il faut raisonner en quantités de matières mélangées, avant de faire intervenir le volume final :
[Ca2+]3 = [Ca2+]1*V'1/V3 = ... mol/L
[Na+]3 = [Na+]2*V2/V3 = ... mol/L
[Cl-]3 = ( [Cl-]1*V'1 + [Cl-]2*V2) /V3 = ... mol/L
Merci pour les fiches
Question 3/5
Mais on ne connait pas la concentration de [H30^+], comment calculer le PH dans ce cas
Question4/1
Ion argent
Question 4/2
AgNO3===> Ag^+ + NO3^-
Question 4/3
Déterminons la quantité de matière de AgNO3
n(Ag)=C4*V4
n(Ag)=10^-2*0,01
n(Ag)=10^-4 mol
Bilan molaire
n(AgNO3)=n(Ag^+)
n(Ag^+) désigné la quantité de matière du précipité
m(AgNO3)=n(Ag^+)*M(Ag^+)
M(Ag^+)=108 g/mol
m(AgNO3)=10^-4*108
m(AgNO3)=1,1*10^-2 g
Question 3/5
Dans ce cas
PH=7
Encore une fois il faut davantage rédiger !
Question4/1
Ion argent
Question 4/2
AgNO3===> Ag^+ + NO3^-
Question 4/3
Déterminons la quantité de matière de AgNO3
n(Ag)=C4*V4
n(Ag)=10^-2*0,01
n(Ag)=10^-4 mol
Bilan molaire
n(AgNO3)=n(Ag^+)
n(Ag^+) désigné la quantité de matière du précipité
m(AgNO3)=n(Ag^+)*M(Ag^+)
M(Ag^+)=108 g/mol
m(AgNO3)=10^-4*108
m(AgNO3)=1,1*10^-2 g
Non, non et non !
Je souhaite avoir un schéma puis un tableau d'avancement de la réaction et des phrases pour expliquer ce que tu fais
Bonsoir
La méthode que vous avez demandé, c est peu difficile, mais ne vous n inquiète pas ,je vais propose quelque chose
Je cherche toujours
Il n'y a rien de compliqué !
1) Tu t'inspires du schéma que j'avais proposé pour la partie 3 : à quoi ça sert ?
A définir toutes les notations utilisées et à rappeler toutes les données essentielles de l'énoncé => gain de temps le jour d'un examen et diminution du risque d?ambiguïté, d'incompréhension ...
2) Tu détermines les quantités de matière des réactifs à l'état initial
3) Tu fais un tableau d'avancement de la réaction
4) Tu déduis l'avancement final de la réaction
5) Tu conclus.
L'intérêt de rédiger un minimum est aussi de faciliter le travail du correcteur => il gagne du temps le jour d'un examen et sera donc plus conciliant si tu fais une faute d'inattention


