Inscription / Connexion Nouveau Sujet
Chimie
Bonjour,
J'ai un problème de compréhension de mon exercice de chimie svp aidez moi à résoudre et à comprendre.
Le polyacétate de vinyle est une matière plastique fabriqué industriellement par la polymérisation de l'acétate de vinyle de formule semi-développée:
CH3COOCH=CH2
1- Dire pourquoi l'acétate de vinyle est polymérisable.
2- donne le motif du polyacétate de vinyle.
3- Écris l'équation de polymérisation de l'acétate de vinyle.
4- Le polyacétate de vinyle à une masse molaire de Mp=129kg/mol. Calculer son degré de polymérisation.
Données : M(c)=12g/mol;M(H)=1g/mol;M(o)=16g/mol.
Bonjour
Cet exercice est une application directe du cours...
Suggestion : commence par expliquer ce que tu es capable de faire et ce qui te bloque. L'aide qui pourra t'être apportée ensuite te sera plus profitable qu'un simple corrigé pas nécessairement adapté à ton niveau.
1. l'acétate de vinyle est polymérisation car il, il contient la double liaison C=C
2. Le motif -CH-CH2-
Soit tu n'as pas compris, soit tu ne réussis pas à représenter sur ce forum les formules semi développées. Étudie bien le schéma ci-dessous. Il faut partir de n molécules d'acétate de vinyle. Dans une première étape, une des deux liaisons de la double liaison carbone - carbone se brise. Tu dois savoir qu'une liaison covalente résulte de la mise en commun de deux électrons entre deux atomes. Chacun des deux atomes C récupère ainsi un électron, représenté par un "point" sur le schéma. Cet électron est ainsi disponible pour que l'atome C établisse une nouvelle liaison covalente avec un autre groupement. On va ainsi obtenir une molécule très longue. "n" est le degré de polymérisation. On peut considérer la polymérisation comme une succession d'un grand nombre de réactions d'addition... Il faut que tu revois ton cours...
Remarque : petit problème avec mon logiciel de dessin : toutes les liaisons C-C du polymère sont de même longueur.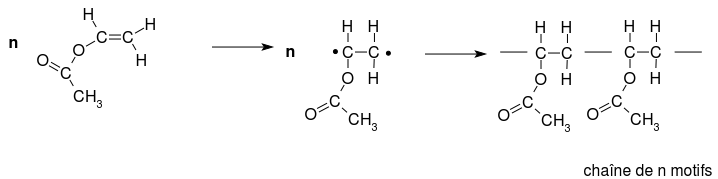
***Image recadrée***
Commence par calculer la masse molaire d'un motif. Ayant la masse molaire du polymère, une simple division te donnera la valeur de n...


